Tamaño del mercado de pruebas de seguridad biológica, participación y análisis de la industria, por productos y servicios (kits y reactivos, instrumentos y servicios), por tipo de prueba (esterilidad, endotoxinas/pirógenos, micoplasma, carga biológica, seguridad viral/agentes adventicios, HCP/HCDNA residual, caracterización de líneas celulares y otros), por aplicación (mAbs y proteínas recombinantes, vacunas, terapias celulares y genéticas, sangre y productos de plasma y productos de tejidos/células madre), por usuario final (empresas farmacéuticas y de biotecnología, CRO/CDMO, institutos acad
Tamaño del mercado de pruebas de seguridad de productos biológicos y perspectivas futuras
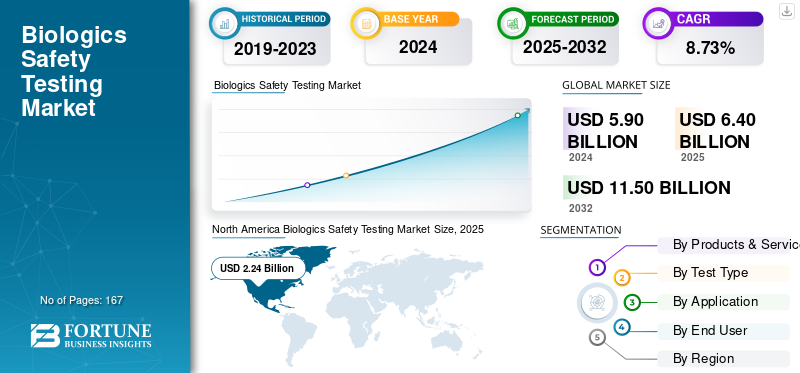
El tamaño del mercado mundial de pruebas de seguridad de productos biológicos se valoró en 5,90 mil millones de dólares en 2024. Se proyecta que el mercado crecerá de 6,40 mil millones de dólares en 2025 a 11,50 mil millones de dólares en 2032, exhibiendo una tasa compuesta anual del 8,73% durante el período previsto.
Se prevé que el mercado de pruebas de seguridad de productos biológicos experimente un crecimiento significativo debido al aumento exponencial en la producción de productos biológicos ybiosimilares, cuyo objetivo es hacer frente a la creciente carga de morbilidad. Se prevé que este aumento de producción dará como resultado una creciente adopción de productos biológicos, consumibles para pruebas de seguridad y otros servicios. Las economías en desarrollo están surgiendo como un centro potencial para la subcontratación de pruebas de seguridad. Haciendo hincapié en las oportunidades que presentan estos factores, muchos actores importantes se están centrando en ampliar sus capacidades de pruebas biológicas mediante el lanzamiento de instalaciones en todo el mundo.
- Por ejemplo, en noviembre de 2023, Merck KGaA completó la segunda fase de su nuevo Centro de Pruebas Biológicas de 39,4 millones de dólares en China, ampliando el laboratorio en 1.500 metros cuadrados, que se inauguró en 2024. El desarrollo permitió a los clientes acceder a una amplia gama de servicios de pruebas para la caracterización de líneas celulares y la liberación de lotes desde el desarrollo preclínico hasta la comercialización.
Además, el mercado está dominado por varios actores operativos clave, incluidos Merck KGaA, SGS Société Générale de Surveillance SA, Thermo Fisher Scientific Inc. y Sartorius AG, que dirigen sus recursos hacia fusiones y adquisiciones estratégicas para fortalecer su posición en el mercado.
Descargar muestra gratuita para conocer más sobre este informe.
DINÁMICA DEL MERCADO
IMPULSORES DEL MERCADO:
Crecimiento exponencial de productos biológicos, en particular terapias celulares y genéticas, para impulsar el crecimiento del mercado
Con los avances en productos biológicos, como las modalidades de terapia celular y génica, también está aumentando la necesidad de pruebas de seguridad rigurosas y de alta frecuencia, lo que impulsa directamente el crecimiento del mercado mundial de pruebas de seguridad de productos biológicos. Los pasos de fabricación involucrados en estos productos biológicos de próxima generación están asociados con altos riesgos de contaminación y requieren estrictos protocolos de pruebas de seguridad en cada etapa de la producción.
El aumento de los ensayos clínicos de terapias celulares y genéticas está impulsando aún más la demanda de perfiles de seguridad validados. Además, muchos actores clave se están centrando en los avances tecnológicos para respaldar la demanda global de pruebas de seguridad de productos biológicos y capitalizar su posición en el mercado.
- Por ejemplo, en agosto de 2025, ViruSure, líder mundial en pruebas de seguridad de patógenos para productos biofarmacéuticos, y Oxford Nanopore Technologies, la compañía detrás de una nueva generación de tecnología de detección molecular basada en nanoporos, anunciaron el lanzamiento de la primera prueba de detección de agentes virales adventicios (AVA) validada por buenas prácticas de laboratorio (GLP) de la industria que utiliza tecnología de secuenciación basada en nanoporos. Se espera que estos acontecimientos críticos impulsen el crecimiento del mercado.
RESTRICCIONES DEL MERCADO:
Restricciones de infraestructura y talento para impedir el crecimiento del mercado
Uno de los factores destacados que obstaculiza la adopción generalizada de estos servicios incluye la disponibilidad limitada de infraestructura de alto nivel y talento especializado. Estos servicios avanzados a menudo requieren la presencia de laboratorios BSL-2/BSL-3, equipos de procesamiento posterior tecnológicamente superiores, sistemas robustos de integridad de datos e infraestructura de TI validada, lo que a menudo contribuye a aumentar los costos. Además, estos servicios y productos requieren un gasto de capital inicial, profesionales capacitados con equipos especializados y un cumplimiento estricto de los estándares regulatorios y de seguridad, lo que aumenta los tiempos de entrega y la carga operativa. En conjunto, estos factores aumentan los costos de implementación y ralentizan la adopción, lo que obstaculiza el crecimiento del mercado.
- Por ejemplo, en octubre de 2025, Cytiva lanzó su tercer Índice Global de Biofarmacia e informó que aproximadamente un tercio de los ejecutivos experimentan una escasez grave o crítica en áreas clave asociadas con modalidades farmacológicas avanzadas, como terapias celulares y genéticas, ARNm y conjugados de anticuerpos y fármacos (ADC), sostenibilidad, fabricación, habilidades digitales y de inteligencia artificial. Estos factores impactan negativamente el crecimiento del mercado.
OPORTUNIDADES DE MERCADO:
Cambio hacia sistemas de microbiología rápidos y automatizados para aumentar la eficiencia y ofrecer oportunidades de crecimiento lucrativas
Una de las oportunidades destacadas para el crecimiento del mercado es el cambio cada vez mayor hacia sistemas de microbiología rápidos y automatizados que ofrecen eficiencia en las pruebas de seguridad de productos biológicos. Estos sistemas automatizados ofrecen varios beneficios sobre los métodos tradicionales, como pruebas rápidas de esterilidad y detección microbiana en tiempo real.sensoresy contadores de colonias habilitados para IA. Estas características reducen significativamente los plazos de control de calidad, lo que permite la detección rápida de contaminación. Estos ayudan a reducir el tiempo de respuesta de los productos biológicos con vidas útiles más cortas, como las terapias celulares y genéticas. Varias empresas clave se están asociando para utilizar este tipo de plataformas automatizadas y aumentar su eficiencia.
- Por ejemplo, en enero de 2024, Rapid Micro Biosystems, Inc. se asoció con Samsung Biologics, utilizando su plataforma Growth Direct, para la automatización de procesos de control de calidad microbiana. Esta asociación tenía como objetivo ofrecer una integridad de datos más sólida, mayor eficiencia y operaciones de control de calidad escalables. Esta colaboración estratégica impulsa el crecimiento del mercado.
TENDENCIAS DEL MERCADO DE PRUEBAS DE SEGURIDAD DE BIOLÓGICOS:
El cambio hacia las pruebas sin animales es una tendencia destacada del mercado
Una de las tendencias destacadas observadas en el mercado es un cambio hacia métodos microbiológicos rápidos (RMM) y ensayos de pruebas de endotoxinas sin animales, a medida que los fabricantes se esfuerzan por realizar pruebas de calidad más éticas. Los métodos tradicionales de prueba de seguridad dependían en gran medida de componentes de origen animal, lo que planteaba preocupaciones sobre la sostenibilidad. Estos factores alentaron a las empresas a adoptar plataformas automatizadas de detección microbiana y ensayos de endotoxinas del factor C recombinante (rFC), que reducen las pruebas y al mismo tiempo disminuyen la dependencia de componentes de origen animal. Los principales actores del mercado han aumentado la adopción de estos RMM y ensayos recombinantes. A medida que se expanden los productos biológicos, estas tecnologías ayudan a acortar los ciclos de liberación de lotes, mejorar la consistencia y consolidarlos como una tendencia clave de la industria.
- Por ejemplo, en abril de 2025, Schrödinger, Inc. apoyó a la FDA de EE. UU. para reducir, refinar o potencialmente reemplazar los requisitos actuales de pruebas con animales con nuevos enfoques para mejorar la seguridad de los medicamentos y acelerar el proceso de evaluación, al tiempo que se reduce la experimentación con animales.
DESAFÍOS DEL MERCADO:
Las regulaciones estrictas y el alto escrutinio por parte de los organismos reguladores plantean un desafío importante para el crecimiento del mercado
Uno de los desafíos importantes que enfrenta el mercado es el creciente riesgo de contaminación microbiana, que resulta en un escrutinio por parte de los organismos reguladores. Aumenta la carga operativa y financiera de los fabricantes. Estos requisitos se vuelven más rigurosos a medida que las terapias biológicas y basadas en células crecen en complejidad, lo que exige tecnologías de prueba más rigurosas e instalaciones mejoradas. El incumplimiento de estas pautas genera retrasos en las aprobaciones y plazos extendidos para el lanzamiento del producto.
Además, cualquier incidente de contaminación menor desencadena una acción regulatoria inmediata, deteniendo la producción, obligando a la destrucción de lotes y perjudicando los plazos. Estos factores frenan la innovación y restringen la capacidad de escalar de los actores emergentes, lo que restringe el crecimiento del mercado global.
- Por ejemplo, en enero de 2025, la FDA de EE. UU. inspeccionó y emitió una carta de advertencia a Sanofi para su instalación de fabricación de medicamentos de Genzyme Corporation. La carta de advertencia resumía las desviaciones de las buenas prácticas de fabricación actuales (CGMP) para ingredientes farmacéuticos activos (API) y otras fallas de calidad, incluida la caracterización de partículas y la contaminación microbiana.
Descargar muestra gratuita para conocer más sobre este informe.
Análisis de segmentación
Por productos y servicios
El segmento de servicios lideró el mercado con la creciente adopción de la terapia celular y génica
Según los productos y servicios, el mercado se segmenta en kits y reactivos, instrumentos y servicios.
Para saber cómo nuestro informe puede ayudar a optimizar su negocio, Hable con un analista
En 2025, se prevé que el segmento de servicios domine la cuota de mercado mundial de pruebas de seguridad de productos biológicos. El crecimiento del segmento se atribuye a la creciente adopción de la terapia celular y genética, así como a la tendencia creciente de subcontratar servicios de pruebas de seguridad para estas tecnologías innovadoras. Estas terapias requieren productos biológicos complejos, infraestructura avanzada, instalaciones que cumplan con las GMP y otros equipos especializados para realizar pruebas de seguridad avanzadas, lo que exige métodos validados y experiencia en documentación regulatoria. A medida que las agencias reguladoras endurecen los estándares, las empresas dependen cada vez más de estos servicios de subcontratación para realizar diversos servicios de pruebas de seguridad. Estos factores impulsan el crecimiento del mercado.
- Por ejemplo, en diciembre de 2024, Eurofins PHAST GmbH ayudó a sus clientes a detectar y controlar antes las impurezas en los medicamentos. Esta entrega oportuna de estos servicios de subcontratación reduce el tiempo de respuesta y respalda el crecimiento segmentario.
Por otro lado, se espera que el segmento de kits y reactivos crezca a una tasa compuesta anual del 9,03% durante el período previsto.
Por tipo de prueba
Fuerte demanda de pruebas de seguridad viral para impulsar el dominio del segmento de seguridad viral/agentes adventicios
Según el tipo de prueba, el mercado se clasifica en esterilidad, endotoxina/pirógeno, micoplasma, carga biológica, seguridad viral/agentes adventicios, HCP/HCDNA residual, caracterización de líneas celulares y otros.
Entre ellos, se estima que el segmento de seguridad viral/agentes adventicios tendrá la mayor participación del mercado, con un 27,8%, en 2025. Las pruebas de seguridad viral son el componente más crítico de la fabricación de productos biológicos y las pruebas de seguridad. Los organismos reguladores exigen pruebas exhaustivas de seguridad viral para cada etapa de producción. Estas evaluaciones de seguridad viral son complejas, costosas y requieren muchos métodos para garantizar la seguridad. Con el aumento de la investigación y el desarrollo en la fabricación de vacunas, lasemiconductorSe espera que la industria experimente un crecimiento significativo. Estos factores han alentado a muchos actores clave a invertir en lanzamientos de nuevos productos, investigación y desarrollo, e impulsar el crecimiento del segmento.
- Por ejemplo, en septiembre de 2023, Charles River Laboratories International, Inc., en colaboración con PathoQuest SAS, publicó los resultados positivos de un estudio fundamental en Vaccine. Este estudio demostró que el ensayo de grado GMP de la empresa tenía una mayor capacidad para detectar contaminantes virales en comparación con los ensayos in vivo.
Se espera que el segmento de caracterización de líneas celulares crezca a una tasa compuesta anual del 9,82% durante el período previsto.
Por aplicación
Demanda considerable de anticuerpos monoclonales para impulsar el dominio segmentario
Según la aplicación, el mercado se segmenta en anticuerpos monoclonales (mAb) y proteínas recombinantes, vacunas, terapias celulares y genéticas, productos de sangre y plasma, y productos de tejidos/células madre.
Se espera que el segmento de mAbs y proteínas recombinantes represente la mayor participación del mercado, con un 47,23%, en 2025. Las pruebas de seguridad viral son el componente más crítico de la fabricación y las pruebas de seguridad de productos biológicos. Los organismos reguladores exigen pruebas exhaustivas de seguridad viral para cada etapa de producción. Estas evaluaciones de seguridad viral son complejas, costosas y requieren muchos métodos para garantizar la seguridad. Con el creciente enfoque en la investigación y el desarrollo para la fabricación de vacunas, se espera que el segmento experimente un crecimiento significativo. Estos factores han alentado a muchos actores clave a invertir en el lanzamiento de nuevos productos, impulsando el crecimiento del segmento.
- Por ejemplo, en agosto de 2024, Cygnus Technologies colaboró con TriLink BioTechnologies para lanzar los kits de cuantificación de ADN de células huésped AccuRes de Cygnus. La tecnología se utiliza para desarrollar un ensayo que ayuda a producir bioterapéuticos más seguros y estables, incluidas vacunas.
Se espera que el segmento de vacunas crezca a una tasa compuesta anual del 8,82% durante el período previsto.
Por usuario final
Aumento de las actividades de bioprocesamiento para impulsar el crecimiento segmentario de las empresas farmacéuticas y de biotecnología
Según el usuario final, el mercado se clasifica en empresas farmacéuticas y de biotecnología, CRO/CDMO, institutos académicos y de investigación y laboratorios gubernamentales/reguladores.
Elfarmacéuticay el segmento de empresas de biotecnología está preparado para dominar el mercado con una participación del 51,2% en 2025. Estas empresas son los principales desarrolladores, fabricantes y comercializadores de estos productos biológicos y requieren perfiles de seguridad intensivos de sus candidatos. En estas instalaciones se llevan a cabo intensos controles de calidad, de acuerdo con las directrices de diversos organismos reguladores, durante todo el proceso de desarrollo y producción. Operan con grandes capacidades de fabricación, realizan diversos ensayos clínicos y participan en investigación y desarrollo, lo que facilita la adopción de estos consumibles de pruebas de seguridad e impulsa la demanda. Estos factores alientan a empresas clave a ampliar sus centros de pruebas de bioseguridad y adquirir la certificación GMP, lo que amplifica aún más su volumen de pruebas y fortalece su dominio en el mercado.
- Por ejemplo, en agosto de 2024, WuXi Biologics inauguró cuatro instalaciones de fabricación y el Centro de pruebas de bioseguridad de Suzhou en China, y recibió certificados de Buenas Prácticas de Fabricación (GMP) de la Agencia Europea de Medicamentos (EMA).
Se espera que el segmento CRO/CDMO crezca a una tasa compuesta anual del 7,46% durante el período previsto.
Perspectivas regionales del mercado de pruebas de seguridad de productos biológicos
Por geografía, el mercado se clasifica en Europa, América del Norte, Asia Pacífico, América Latina y Medio Oriente y África.
América del norte
América del Norte tuvo la participación dominante en 2024, valorada en 2.240 millones de dólares, y se prevé que mantenga su posición de liderazgo en 2025, con un valor de 2.010 millones de dólares. La región dominó el mercado con una CAGR significativa, debido a la presencia de un gran número de empresas farmacéuticas y una cartera en expansión de productos biológicos y terapias celulares y genéticas. Estos factores impulsan la demanda de pruebas de seguridad de productos biológicos en el mercado. Se estima que en 2025 el mercado estadounidense alcanzará los 2.150 millones de dólares. Además, Estados Unidos es el epicentro de terapias y experiencias innovadoras, y la creciente inversión en investigación y desarrollo intensifica la demanda del mercado.
- Por ejemplo, en octubre de 2024, Abzena amplió sus capacidades de prueba de control de calidad (QC) en su sitio de fabricación cGMP. El nuevo espacio de laboratorio mejoró el conjunto de herramientas analíticas de anticuerpos de la empresa, ofreciendo pruebas rápidas de liberación microbiológica y una escalabilidad mejorada mediante la separación avanzada de materiales. Estos desarrollos impulsan el crecimiento del mercado.
Europa y Asia Pacífico
Se espera que regiones como Europa y Asia Pacífico experimenten un crecimiento notable en los próximos años. Durante el período previsto, se prevé que la región europea registre una tasa de crecimiento del 7,81%, la segunda más alta entre todas las regiones, y alcance una valoración de 1.840 millones de dólares estadounidenses para 2025. Este crecimiento está impulsado principalmente por el aumento de las terapias avanzadas en toda Europa y la expansión de las capacidades de pruebas de bioseguridad por parte de actores clave en la región. Respaldado por estos factores, se prevé que el Reino Unido registre una valoración de 290 millones de dólares, Alemania de 420 millones de dólares y Francia de 260 millones de dólares en 2025. Después de Europa, la industria de pruebas de seguridad de productos biológicos de Asia Pacífico registrará una valoración de 1,650 millones de dólares en 2025 y aseguró la posición de la tercera región más grande del mercado. En la región, India y China están preparadas para alcanzar valoraciones de 170 millones de dólares y 660 millones de dólares, respectivamente, en 2025.
América Latina, Medio Oriente y África
Durante el período previsto, se espera que las regiones de América Latina y Oriente Medio y África sean testigos de un crecimiento moderado en este espacio de mercado. Se espera que el mercado latinoamericano, en 2025, alcance una valoración de 320 millones de dólares. Se espera que el aumento de la producción de productos biológicos en la región impulse el crecimiento. En Oriente Medio y África, se prevé que el CCG alcance una valoración de 0,09 mil millones de dólares en 2025.
PAISAJE COMPETITIVO
Actores clave de la industria:
Las colaboraciones estratégicas de actores clave respaldaron sus posiciones de liderazgo
El mercado de pruebas de seguridad de productos biológicos muestra una estructura concentrada, con unas pocas empresas que operan activamente en todo el mundo. Estos actores participan activamente en la expansión de la capacidad, el lanzamiento de nuevos productos, las asociaciones estratégicas, las fusiones y adquisiciones y la expansión geográfica. Invierten activamente en avances tecnológicos y ofrecen una amplia gama de ofertas de productos para sistemas innovadores de visión por computadora.
Merck KGaA, SGS Société Générale de Surveillance SA, Thermo Fisher Scientific Inc., Waters Corporation y Lonza son algunos de los actores importantes del mercado. Una amplia gama de diversos productos y servicios de pruebas de seguridad biológica para las pruebas de diversos tipos de productos biológicos contribuirá en gran medida a la cuota de mercado de estas empresas.
- Por ejemplo, en julio de 2025, Waters Corporation colaboró con BD para combinar el negocio de soluciones de diagnóstico y biociencias de BD con Waters, creando un líder en diagnóstico y ciencias biológicas centrado en pruebas reguladas de alto volumen.
Aparte de esto, otros actores destacados en el mercado incluyen Charles River Laboratories, BD y otros. Estas empresas están llevando a cabo diversas iniciativas estratégicas, como inversiones en I+D para mejorar su presencia en el mercado.
LISTA DE EMPRESAS CLAVE DE PRUEBAS DE SEGURIDAD DE BIOLÓGICOS PERFILADAS:
- Merck KGaA(Alemania)
- SGS Société Générale de Surveillance SA (Suiza)
- Thermo Fisher Scientific Inc. (EE. UU.)
- BD (Estados Unidos)
- Sartorius AG(Alemania)
- Laboratorios del río Charles(A NOSOTROS.)
- Eurofins Científico (Luxemburgo)
- Lonza (Suiza)
- Waters Corporation (EE.UU.)
- Reading Scientific Services Ltd (EE. UU.)
- Abzená (Estados Unidos)
DESARROLLOS CLAVE DE LA INDUSTRIA:
- Octubre de 2025:Charles River Laboratories International, Inc. colaboró con Toxys. La colaboración proporcionó a la empresa acceso a ReproTracker, un ensayo in vitro basado en células madre humanas que identifica de forma rápida y fiable los peligros de toxicidad para el desarrollo asociados con nuevos medicamentos y productos químicos.
- Septiembre de 2025:Bionique Testing Laboratories LLC (Bionique), una subsidiaria de Asahi Kasei, amplió sus instalaciones para apoyar aún más el desarrollo de fármacos y satisfacer la demanda de soluciones rápidas de pruebas de bioseguridad.
- Julio de 2025:Creative Diagnostics lanzó sus kits ELISA HCP para mamíferos. Estos kits de ensayo avanzados proporcionaron una detección sensible y confiable de proteínas de la célula huésped (HCP) en biofarmacéuticoprocesos de desarrollo y fabricación. Se utilizan para detectar y cuantificar proteínas residuales de la célula huésped que pueden contaminar productos biológicos durante el proceso de producción.
- Mayo de 2025:Creative Diagnostics lanzó un kit ELISA de ARN polimerasa T7 altamente sensible para la detección de impurezas biofarmacéuticas.
- Octubre de 2024:Merck KGaA inauguró una nueva instalación de pruebas de bioseguridad en Rockville, Maryland, EE. UU.
- Agosto de 2024:Cygnus Technologies colaboró con TriLink BioTechnologies para lanzar los kits de cuantificación de ADN de células huésped AccuRes de Cygnus. La tecnología se utiliza para desarrollar un ensayo que ayude a producir bioterapéuticos más seguros y estables, incluidas vacunas.
COBERTURA DEL INFORME
El análisis de mercado proporciona un estudio completo del tamaño del mercado y el pronóstico para todos los segmentos de mercado incluidos en el informe. Incluye detalles sobre la dinámica del mercado y las tendencias que se espera que impulsen el mercado durante el período de pronóstico. También proporciona descripciones generales de los avances tecnológicos, desarrollo de productos, desarrollos clave de la industria, fusiones y adquisiciones, e información estratégica sobre el crecimiento del mercado. El informe de investigación de mercado también incluye un panorama competitivo detallado, proporcionando información sobre la participación de mercado y los perfiles de los actores operativos clave.
Solicitud de personalización para obtener un conocimiento amplio del mercado.
Alcance y segmentación del informe
| ATRIBUTO | DETALLES |
| Período de estudio | 2019-2032 |
| Año base | 2024 |
| Período de pronóstico | 2025-2032 |
| Período histórico | 2019-2023 |
| Índice de crecimiento | CAGR del 8,73% entre 2025 y 2032 |
| Unidad | Valor (millones de dólares) |
| Segmentación |
Por productos y servicios
Por tipo de prueba
Por aplicación
Por usuario final
Por geografía
|
Preguntas frecuentes
Fortune Business Insights dice que el valor del mercado global se situó en 5.900 millones de dólares en 2025 y se prevé que alcance los 11.500 millones de dólares en 2032.
En 2025, el valor del mercado de América del Norte se situó en 2.240 millones de dólares.
Se espera que el mercado muestre una tasa compuesta anual del 8,73% durante el período previsto de 2025-2032.
Se espera que el segmento de servicios lidere el mercado de subproductos y servicios en 2025.
La creciente producción de productos biológicos y terapias celulares y genéticas son los factores clave que impulsan el mercado.
Merck KGaA, SGS Société Générale de Surveillance SA, Thermo Fisher Scientific Inc., BD y Sartorius AG se encuentran entre los actores destacados del mercado.
América del Norte dominó el mercado en 2024.
Póngase en contacto con nuestras expertas Habla con un experto
Obtenga un 20% de personalización gratuita
Ampliar la cobertura regional y por país, Análisis de segmentos, Perfiles de empresas, Benchmarking competitivo, e información sobre el usuario final.
Informes relacionados