Tamanho do mercado de validação de bioprocessos, participação e análise da indústria, por tipo de teste (testes extraíveis e lixiviáveis, testes microbiológicos, testes de compatibilidade, testes de integridade, testes fisioquímicos, & outros), por modo (interno e terceirizado), por área de validação (validação de processos, validação de limpeza, validação de método analítico, qualificação de equipamentos, & outros), por farmacêutico (anticorpos monoclonais, proteínas recombinantes, Vacinas, terapias celulares e genéticas, biossimilares e outros), por usuário final (empresas farmacêuti
Visão geral do mercado de validação de bioprocessos
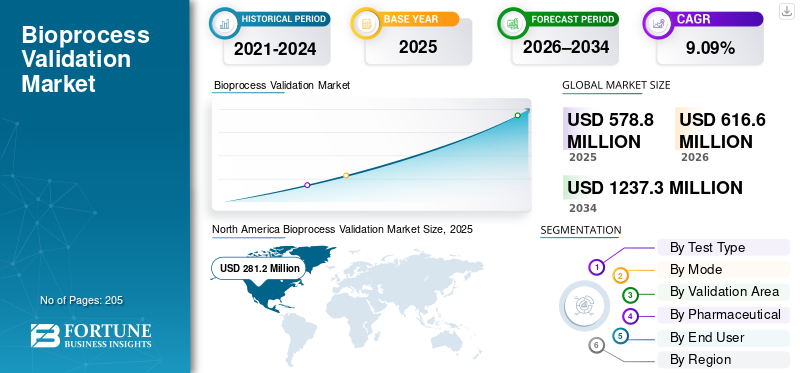
O tamanho global do mercado de validação de bioprocessos foi avaliado em US$ 578,8 milhões em 2025. O mercado deve crescer de US$ 616,6 milhões em 2026 para US$ 1.237,3 milhões até 2034, exibindo um CAGR de 9,09% durante o período de previsão.A América do Norte dominou o mercado de validação de bioprocessos com uma participação de mercado de 48,58% em 2025.
A validação de bioprocessos garante que os processos de fabricação biofarmacêutica produzam consistentemente produtos biológicos seguros e eficazes. É a prova documentada de que um processo de biofabricação, como a produção de um anticorpo monoclonal, vacina, célula/terapia genética, ou proteína recombinante, produzirá consistentemente um produto que atenda aos atributos de qualidade do produto predefinidos e aos requisitos regulatórios na escala comercial pretendida. Este mercado está crescendo significativamente devido ao maior foco no desenvolvimento de produtos biológicos inovadores.
Os principais players do mercado incluem Merck KGaA, Eurofins Scientific, SGS Société Générale de Surveillance SA, Sartorius AG, entre outros. Essas empresas estão focadas em avanços tecnológicos em suas ofertas de serviços.
Descarregue amostra grátis para saber mais sobre este relatório.
TENDÊNCIAS DE MERCADO DE VALIDAÇÃO DE BIOPROCESSOS
A terceirização para CDMOs é uma tendência de mercado proeminente
Nos últimos anos, o mercado está mudando da validação interna para serviços de validação terceirizados. O trabalho de validação de bioprocessos está se tornando mais especializado, enquanto as empresas buscam prazos mais rápidos e capacidade variável, em vez de expandir permanentemente equipes internas de controle de qualidade/validação. À medida que a presença da biofabricação se globaliza, as empresas também terceirizam para garantir documentação consistente de GMP, execução padronizada e dados prontos para auditoria em todos os locais. A tendência é especialmente forte durante transferências de tecnologia, expansões de capacidade, projetos de remediação e quando as equipes internas enfrentam restrições de largura de banda. Além disso, a terceirização também reduz a carga de custos fixos e fornece acesso a conhecimentos de nicho e instrumentação de ponta cuja manutenção interna é cara. Esses fatores estão apoiando o crescimento global do mercado global de validação de bioprocessos.
- Por exemplo, em outubro de 2024, a SGS anunciou uma expansão das capacidades de testes biofarmacêuticos em sua unidade em Lincolnshire, nos EUA, observando explicitamente que a instalação atualmente fornece serviços de terceirização para desenvolvedores e fabricantes nos setores farmacêutico, biofarmacêutico edispositivo médico
Descarregue amostra grátis para saber mais sobre este relatório.
DINÂMICA DE MERCADO
MOTORIZADORES DE MERCADO
O aumento do pipeline global de produtos biológicos e biossimilares, aumentando a demanda de validação, está impulsionando o crescimento do mercado
O mercado está sendo impulsionado principalmente pela rápida expansão dos produtos biológicos ebiossimilaresgasoduto. Isso se deve ao fato de cada nova molécula passar do desenvolvimento para a escala comercial, desencadeando validação de processo fresco (PPQ/CPV), validação/transferência de método analítico, validação de limpeza e extensa documentação para prontidão para GMP. À medida que os patrocinadores adicionam mais ativos biossimilares, eles também aumentam o trabalho de comparabilidade, os controles de alterações e as transferências de tecnologia entre locais/CDMOs, cada etapa exigindo suporte de validação para provar consistência e controle. Além disso, o aumento das colaborações entre empresas operacionais também apoia a expansão do mercado.
- Por exemplo, em julho de 2024, a Evotec expandiu a sua parceria estratégica com a Sandoz para o desenvolvimento e produção comercial de biossimilares.
RESTRIÇÕES DE MERCADO
Alta complexidade analítica e necessidade de expertise técnica especializada para dificultar o crescimento do mercado
A elevada complexidade analítica é uma restrição do mercado, uma vez que produtos biológicos, vacinas e CGT requerem frequentemente um amplo painel de ensaios sensíveis, e cada método deve ser validado, transferido e mantido num estado controlado em todos os locais. Isto eleva o custo e o tempo dos projetos de validação e torna a execução dependente de escassos especialistas. Quando há falta de conhecimento profundo, problemas de robustez do método e lacunas de documentação podem desencadear desvios, repetição de estudos e atrasos na liberação de lotes ou cronogramas de transferência de tecnologia, retardando diretamente o arranque do programa. A mesma complexidade também aumenta a dependência de instrumentação de ponta e de tratamento de dados sofisticado, que os participantes mais pequenos podem ter dificuldade em manter internamente. Como resultado, os projetos podem gerar gargalos em torno da capacidade especializada, inflacionando os preços dos serviços e estendendo os prazos de entrega. Isso resulta em limitar o crescimento do mercado até certo ponto.
- Por exemplo, em março de 2025, a FDA dos EUA emitiu uma carta de advertência à Aspen Biopharma Labs Private Limited sobre deficiências, incluindo práticas inadequadas de validação de métodos analíticos, observando que tais falhas aumentam o risco de defeitos na qualidade dos medicamentos.
OPORTUNIDADES DE MERCADO
Adoção de tecnologias de uso único para oferecer oportunidades lucrativas para expansão do mercado
A adoção de tecnologias de uso único (SUTs) é uma forte oportunidade de mercado para prestadores de serviços de validação. Cada novo caminho de fluxo descartável aumenta a necessidade de evidências de extraíveis e lixiviáveis (E&L), integridade e compatibilidade para satisfazer as expectativas de GMP. À medida que os fabricantes ampliam o uso de SUT da DP para conjuntos comerciais, eles precisam cada vez mais de pacotes de validação padronizados e repetíveis, em vez de estudos únicos. A oportunidade é especialmente atraente em instalações multiprodutos lideradas por CDMO, onde trocas frequentes e mudanças de fornecedor criam cargas de trabalho de validação recorrentes. No geral, a onda SUT expande a base endereçável para validação como serviço além dos testes de laboratório, à medida que os clientes buscam documentação e interpretação prontas para auditoria. Por exemplo, em abril de 2024, a Cytiva revelou o sistema de mistura magnética compacto de uso único Xcellerex para mAb em grande escala,vacinae fabricação de terapia avançada.
DESAFIOS DO MERCADO
Cadeia de suprimentos e restrições de capacidade para laboratórios de testes especializadosRepresenta um desafio proeminente para o crescimento do mercado
As interrupções na cadeia de abastecimento e a capacidade limitada de testes especializados são um desafio persistente do mercado. Os prazos de validação geralmente dependem de vagas escassas no laboratório, longos prazos de entrega para consumíveis/reagentes e a disponibilidade de analistas treinados. Quando os laboratórios enfrentam picos repentinos de demanda, os atrasos aumentam os prazos de entrega, atrasando a liberação de lotes, cronogramas de PPQ e arquivamento de pacotes. Além disso, a volatilidade da cadeia de abastecimento também força os laboratórios a qualificar reagentes/materiais alternativos, acrescentando retrabalho e diminuindo o rendimento. Isto é especialmente doloroso para produtos biológicos de alto valor e modalidades de curto prazo de validade, onde a espera pelos testes pode bloquear o envio. Como resultado, os biofabricantes precisam cada vez mais de planos de contingência com vários laboratórios e são empurrados para serviços premium/rápidos, aumentando os custos e a complexidade do planejamento. Todos os fatores afetam cumulativamente o crescimento do mercado.
Análise de Segmentação
Por tipo de teste
Aumento da demanda devido à crescente adoção de SUTs para impulsionar o crescimento do segmento de testes de extraíveis e lixiviáveis
Com base no tipo de teste, o mercado é dividido em testes extraíveis e lixiviáveis, testes microbiológicos e testes de compatibilidade, testes de integridade, testes físico-químicos, entre outros.
O segmento de testes de extraíveis e lixiviáveis capturou a maior participação de mercado global de validação de bioprocessos. A biofabricação mudou fortemente para sistemas de uso único, e cada superfície de contato com polímero cria um risco direto à segurança do paciente e ao risco de adesão que deve ser caracterizado e documentado. À medida que a adoção do SUS vai do desenvolvimento de processos à produção comercial, as empresas precisam de pacotes de E&L repetíveis que sejam normalmente mais especializados e de maior valor do que verificações físicas ou de compatibilidade de rotina. Devido a isso, os players operacionais também estão se concentrando na expansão de suas ofertas de serviços com aprovações regulatórias.
- Por exemplo, em maio de 2025, a SGS anunciou que recebeu a acreditação ISO 17025 para o seu laboratório farmacêutico canadense oferecer testes de extraíveis e lixiviáveis.
Prevê-se que o segmento de testes de integridade aumente com um CAGR de 10,56% durante o período de previsão.
Para saber como nosso relatório pode ajudar a otimizar seu negócio, Fale com um analista
Por modo
Alto investimento na fabricação interna para impulsionar o crescimento segmental interno
Com base na modalidade, o mercado é dividido em interno e terceirizado.
O segmento interno dominou o mercado global em 2025. Grandebiofarmacêuticoos fabricantes preferem manter as principais atividades de validação incorporadas em seu sistema de qualidade. Isso reduz o risco regulatório ao garantir POPs consistentes, aprovações internas mais rápidas e um controle mais rígido sobre a documentação de BPF e decisões sobre impacto em lotes. As equipes internas também protegem o conhecimento/PI do processo, o que é especialmente importante para produtos biológicos, onde pequenas alterações podem afetar os CQAs. É por isso que as empresas que investem em novas instalações biológicas muitas vezes constroem fortes infra-estruturas internas de laboratório/fabricação que exigem inerentemente organizações de validação internas de tamanho considerável. Além disso, o segmento deverá deter 59,6% de participação em 2026.
- Por exemplo, em abril de 2025, a Merck anunciou o lançamento de um Centro de Excelência Biológica de mil milhões de dólares em Wilmington, Delaware, compreendendo capacidades laboratoriais e de produção para apoiar o lançamento e a produção comercial.
Prevê-se que o segmento terceirizado aumente com um CAGR de 10,61% durante o período de previsão.
Por área de validação
Alto uso em validação para impulsionar o crescimento do segmento de qualificação de equipamentos
Com base na área de validação, o mercado é dividido em validação de processos, validação de limpeza, validação de métodos analíticos, qualificação de equipamentos, entre outros.
O segmento de qualificação de equipamentos capturou a maior parcela do mercado global em 2025. É uma etapa obrigatória para trazer qualquer ativo GMP para equipamentos, e os serviços públicos, e muitas vezes sistemas inteiros de salas limpas, devem ser comprovados como instalados corretamente e operando de forma consistente antes que o trabalho do processo possa ser dimensionado. Ao contrário da validação de processos ou de limpeza, a qualificação é desencadeada por cada nova construção, expansão de capacidade, substituição de equipamento, atualização de automação e controlo de alterações importantes, pelo que ocorre repetidamente ao longo do ciclo de vida de um local. Também exige muita mão-de-obra e abrange múltiplas disciplinas, o que aumenta os gastos com serviços. Além disso, o segmento deverá deter uma participação de 27,5% em 2026.
- Por exemplo, em novembro de 2025, a Exyte concluiu a integração do Pharmaplan para permitir a entrega ponta a ponta de instalações GMP, desde a viabilidade até a entrega qualificada.
Prevê-se que o segmento de validação de métodos analíticos aumente com um CAGR de 10,62% durante o período de previsão.
Por Farmacêutico
A expansão do pipeline de anticorpos monoclonais apoiou a dominância segmentar
Baseado em produtos farmacêuticos, o mercado é dividido em anticorpos monoclonais, proteínas recombinantes, vacinas,terapias celulares e genéticas, biossimilares e outros.
Prevê-se que o segmento de anticorpos monoclonais capture a maior participação de mercado em 2025. Esta é a maior base instalada de fabricação de produtos biológicos comerciais com vários produtos comercializados e um forte pipeline clínico. Além disso, os mAbs estão cada vez mais inseridos em modalidades de maior valor, como portfólios de mAbs e plataformas relacionadas, impulsionando novas instalações, ciclos de qualificação de equipamentos e pacotes de qualificação/validação. Além disso, o segmento deverá deter uma participação de 36,5% em 2026.
- Por exemplo, em setembro de 2025, a Eli Lilly anunciou planos para construir uma fábrica de 5 mil milhões de dólares na Virgínia, descrita como um local dedicado à plataforma emergente de bioconjugados e ao portfólio de anticorpos monoclonais da Lilly.
Prevê-se que o segmento de terapias celulares e genéticas aumente com um CAGR de 16,27% durante o período de previsão.
Por usuário final
Forte expansão de produtos biológicos e investimentos em GMP apoiam o crescimento do segmento de empresas farmacêuticas e de biotecnologia
Com base no usuário final, o mercado é segmentado emfarmacêuticoe empresas de biotecnologia, organizações de desenvolvimento e fabricação de contratos e outras.
Em 2025, o segmento de empresas farmacêuticas e de biotecnologia ocupava a posição de liderança no mercado global. Estas empresas estão ativamente envolvidas no desenvolvimento de portfólios de produtos biológicos e são as maiores operadoras de redes de fabricação de GMP. Além disso, o aumento dos investimentos das empresas biofarmacêuticas apoia o crescimento do segmento. Além disso, deverá deter uma participação de 68,2% em 2026.
- Por exemplo, em setembro de 2025, a Gilead Sciences lançou um novo centro de produção nos EUA para reforçar a sua capacidade e capacidades em produtos biológicos.
Além disso, o segmento de organizações de desenvolvimento e manufatura de contratos deverá crescer a um CAGR de 12,01% durante o período de previsão.
Perspectiva Regional do Mercado de Validação de Bioprocessos
Por geografia, o mercado é segmentado na América do Norte, Europa, Ásia-Pacífico, América Latina e Oriente Médio e África.
América do Norte
North America Bioprocess Validation Market Size, 2025 (USD Million)
Para obter mais informações sobre a análise regional deste mercado, Descarregue amostra grátis
O tamanho do mercado da América do Norte foi de US$ 268,8 milhões em 2024 e dominou o mercado global. A região também manteve o seu domínio em 2025, com 281,2 milhões de dólares. O domínio regional é impulsionado pela rápida expansão de gasodutos biológicos e biossimilares, pelo forte apoio regulamentar e pela presença de CDMOs avançados na região.
Mercado de validação de bioprocessos dos EUA
O mercado dos EUA foi responsável pela maior participação do mercado norte-americano e pode ser analiticamente aproximado em cerca de US$ 273,8 milhões em 2026, representando cerca de 44,4% do mercado global.
Ásia-Pacífico
O tamanho do mercado Ásia-Pacífico está projetado para ser avaliado em US$ 150,1 milhões em 2026. As regiões devem garantir a posição de segunda maior região do setor. Fatores como a rápida expansão da fabricação de produtos biológicos, especialmente na China, na Índia, e os crescentes investimentos em CDMO, são responsáveis pelo crescimento do mercado regional.
Mercado Japonês de Validação de Bioprocessos
O mercado japonês em 2026 está estimado em cerca de 22,1 milhões de dólares, representando cerca de 3,6% das receitas globais.
Mercado de validação de bioprocessos da China
Prevê-se que o mercado da China atinja receitas de cerca de 43,0 milhões de dólares em 2026, representando cerca de 7,0% das vendas globais.
Mercado de validação de bioprocessos da Índia
O mercado da Índia em 2026 está estimado em cerca de 26,2 milhões de dólares, representando cerca de 4,3% das receitas globais.
Europa
Prevê-se que o mercado europeu cresça a um CAGR de 7,70% durante o período de previsão. Prevê-se que a região se torne a terceira maior entre todas as regiões. O mercado regional é impulsionado principalmente pela presença de fortes clusters de biotecnologia, regulamentos de apoio da EMA e expansão dos ecossistemas CDMO em todos os países europeus.
Mercado de validação de bioprocessos do Reino Unido
O mercado do Reino Unido em 2026 é estimado em cerca de 24,8 milhões de dólares, representando cerca de 4,0% das receitas globais.
Mercado de validação de bioprocessos da Alemanha
O tamanho do mercado alemão deverá atingir aproximadamente US$ 29,2 milhões em 2026, equivalente a cerca de 4,7% das vendas globais.
América Latina e Oriente Médio e África
As regiões da América Latina, do Médio Oriente e de África cresceriam a um ritmo relativamente mais lento durante o período de estudo. O tamanho do mercado da América Latina deverá atingir uma avaliação de US$ 28,4 milhões em 2026. Esse crescimento regional é impulsionado principalmente pela biofabricação emergente e pelo aumento da terceirização seletiva nessas regiões.
Entre a região do Médio Oriente e África, o mercado do CCG em 2026 está estimado em cerca de 9,5 milhões de dólares, representando cerca de 1,5% das receitas globais.
CENÁRIO COMPETITIVO
Principais participantes da indústria
Expansões estratégicas em capacidade de testes especializados e ofertas de validação digital estão remodelando o posicionamento competitivo
O mercado global de validação de bioprocessos está moderadamente fragmentado. Os principais participantes incluem Eurofins Scientific, SGS, Nelson Labs (Sotera Health), Charles River Laboratories, Thermo Fisher Scientific Inc., MerckKGaA e Sartorius. Esses participantes estão se concentrando em expansões de capacidade, desenvolvimento de capacidades em extraíveis e lixiviáveis, e garantia de esterilidade, fusões e aquisições para expandir a pegada microbiológica e parcerias para acelerar fluxos de trabalho de validação digitais/habilitados por IA.
- Por exemplo, em junho de 2025, a Nelson Labs anunciou o projeto de expansão para duplicar a capacidade de salas limpas com classificação ISO em sua sede em Salt Lake City para atender à crescente demanda por serviços de garantia de esterilidade e aos rigorosos requisitos do Anexo 1 das BPF da UE.
Outros players importantes do mercado incluem Laboratory Corporation of America Holdings, DOC S.r.l., Hangzhou Cobetter Filtration Equipments Co., Ltd, Meissner Filtration Products, Inc. Essas empresas estão oferecendo ativamente serviços inovadores em diversas aplicações.
LISTA DAS PRINCIPAIS EMPRESAS DE VALIDAÇÃO DE BIOPROCESSOS PERFILADAS
- Merck KGaA(Alemanha)
- Eurofins Científica (Luxemburgo)
- SGS Société Générale de Surveillance SA(Suíça)
- Sartório AG(Alemanha)
- Cytiva (Danaher)(NÓS.)
- Laboratory Corporation of America Holdings (EUA)
- DOC S.r.l. (Itália)
- Equipamentos de filtragem Cobetter Hangzhou Co., Ltd (China)
- Meissner Filtration Products, Inc.
- Laboratórios Charles River. (NÓS.)
PRINCIPAIS DESENVOLVIMENTOS DA INDÚSTRIA
- Dezembro de 2025:Sikich anunciou uma parceria estratégica com a ValGenesis para oferecer a plataforma de validação digital baseada em IA da ValGenesis para clientes de ciências biológicas, modernizando os processos de validação.
- Outubro de 2025:A Intertek Pharmaceutical Services lançou serviços de testes de extraíveis e lixiviáveis (E&L) para apoiar a conformidade com os novos requisitos da Farmacopeia Coreana.
- Outubro de 2025:Alcami anunciou uma expansão de serviços de laboratório de 20.000 pés quadrados em Durham, NC, para fortalecer as capacidades analíticas para produtos biológicos/CGT (estabelecimento de métodos, liberação/estabilidade e caracterização).
- Julho de 2025:ValGenesis anunciou até US$ 16 milhões em financiamento estratégico para acelerar a expansão global e a inovação orientada por IA no gerenciamento do ciclo de vida de validação (validação digital).
- Setembro de 2024:A Pace Life Sciences anunciou a aquisição do laboratório de serviços analíticos da Catalent em RTP, Carolina do Norte, expandindo capacidade/capacidades em serviços analíticos que suportam programas de validação.
COBERTURA DO RELATÓRIO
Pedido de Personalização Para obter informações abrangentes sobre o mercado.
Escopo e segmentação do relatório
| ATRIBUTO | DETALHES |
| Período de estudo | 2021-2034 |
| Ano base | 2025 |
| Ano estimado | 2026 |
| Período de previsão | 2026-2034 |
| Período Histórico | 2021-2024 |
| Taxa de crescimento | CAGR de 9,09% de 2026-2034 |
| Unidade | Valor (US$ milhões) |
| Segmentação | Por tipo de teste, modo, área de validação, farmacêutico, usuário final e região |
| Por tipo de teste |
|
| Por modo |
|
| Por aplicativo |
|
| Por Farmacêutico |
|
| Por usuário final |
|
| Por região |
|
Perguntas Frequentes
De acordo com a Fortune Business Insights, o valor do mercado global situou-se em 578,8 milhões de dólares em 2025 e prevê-se que atinja 1.237,3 milhões de dólares em 2034.
Em 2025, o valor de mercado norte-americano situou-se em 281,2 milhões de dólares.
Espera-se que o mercado apresente um CAGR de 9,09% durante o período de previsão.
Por tipo de teste, o segmento de testes extraíveis e lixiviáveis liderou o mercado.
O crescente pipeline global de produtos biológicos e biossimilares, por sua vez, aumentando a demanda de validação, são os principais fatores que impulsionam o mercado.
Merck KGaA, Eurofins Scientific, SGS Société Générale de Surveillance SA e Sartorius AG são alguns dos players proeminentes no mercado global.
A América do Norte dominou o mercado em 2025 com a maior participação.
Entre em contacto com os nossos especialistas Fale com um especialista
Obtenha 20% de personalização gratuita
Ampliar a cobertura regional e por país, Análise de segmentos, Perfis de empresas, Benchmarking competitivo, e insights sobre o usuário final.
-
US +1 833 909 2966 (chamada gratuita)
-
Entre em contacto connosco