Control de calidad y cumplimiento farmacéutico Tamaño del mercado, participación y análisis de la industria, por oferta (productos {instrumentos y consumibles}, software y servicios), por aplicación (medicamentos de moléculas pequeñas, productos biológicos y biosimilares, vacunas, terapias celulares y genéticas, y otros) por función (control de calidad de materias primas, control de microbiología y contaminación, pruebas de estabilidad y vida útil, control de calidad en proceso, pruebas de productos terminados y liberación de lotes, y otros), por usuario final (Empresas farmacéuticas y de biot
Control de calidad y cumplimiento farmacéutico Tamaño del mercado y perspectivas futuras
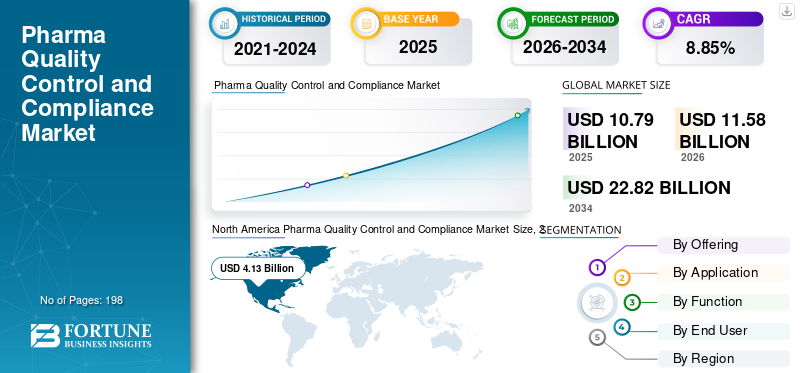
El tamaño del mercado mundial de cumplimiento y control de calidad farmacéutica se valoró en 10,79 mil millones de dólares en 2025. Se proyecta que el mercado crecerá de 11,58 mil millones de dólares en 2026 a 22,82 mil millones de dólares en 2034, exhibiendo una tasa compuesta anual del 8,85% durante el período previsto.
Los sistemas de cumplimiento y control de calidad farmacéutica se utilizan para evaluar la calidad de los medicamentos, garantizar el cumplimiento de las GMP, supervisar la documentación regulada y ayudar en las decisiones de liberación relacionadas con materias primas, lotes en proceso, productos terminados, pruebas microbiológicas, estabilidad y procesos de validación. El mercado se está expandiendo a medida que las empresas farmacéuticas y de biotecnología están impulsando las inversiones en herramientas de control de calidad, consumibles, sistemas de calidad digitales y pruebas GMP subcontratadas para manejar la creciente complejidad de fabricación de moléculas pequeñas, productos biológicos,vacunasy terapias celulares y genéticas. La demanda se ve reforzada aún más por un mayor énfasis en el control de la contaminación, la integridad de los datos, la eficiencia de la liberación de lotes, los procesos de validación y calificación, junto con sistemas de gestión de calidad basados en la nube que mejoran la preparación para las auditorías y el cumplimiento normativo.
Los actores clave que operan en el mercado global incluyen Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation, Sartorius AG y otros. Estas empresas se están centrando en avances tecnológicos en sus productos, colaboraciones estratégicas y expansión de cartera para mantener su presencia en el mercado.
Descargar muestra gratuita para conocer más sobre este informe.
CONTROL DE CALIDAD Y CUMPLIMIENTO FARMACÉUTICO TENDENCIAS DEL MERCADO
El cambio hacia soluciones de cumplimiento automatizadas es una tendencia importante observada en el mercado global
Las empresas farmacéuticas y de biotecnología están pasando de procesos de calidad manuales, basados en papel e inconexos a sistemas automatizados que pueden manejar de manera más consistente las desviaciones, CAPA, gestión de documentos, capacitación, revisión de lotes y preparación para auditorías. Este cambio se produce a medida que los fabricantes regulados requieren una toma de decisiones más rápida, una trazabilidad mejorada, una reducción de los errores de documentación y una mayor integridad de los datos dentro de operaciones cada vez más complejas. Las herramientas de cumplimiento automatizadas ayudan a las empresas a estandarizar los procedimientos en varias ubicaciones, acortar la duración de los ciclos de revisión y mejorar la preparación para inspecciones y auditorías de GMP. La tendencia se está intensificando a medida que aumentan los productos biológicos, los productos estériles y las terapias avanzadas, lo que lleva a un aumento en el volumen de eventos de calidad y documentación de cumplimiento que deben abordarse en tiempo real. En consecuencia, las empresas farmacéuticas están invirtiendo más recursos en eQMS, LIMS, liberación digital de lotes y plataformas de flujo de trabajo impulsadas por IA que vinculan los sistemas regulatorios, de calidad y de fabricación.
- Por ejemplo, en enero de 2025, Honeywell lanzó la plataforma TrackWise Life Sciences, que fue diseñada para transformar la forma en que las organizaciones de ciencias biológicas abordan la fabricación integrada y la gestión de calidad a través de la transformación digital y la automatización avanzada.
DINÁMICA DEL MERCADO
IMPULSORES DEL MERCADO
Descargar muestra gratuita para conocer más sobre este informe.
Aumento de la demanda debido al aumento de las actividades de desarrollo de fármacos para impulsar el crecimiento del mercado
La creciente necesidad derivada del aumento de las actividades de desarrollo de fármacos es un factor importante que impulsa el crecimiento del mercado de cumplimiento y control de calidad farmacéutica. Las empresas farmacéuticas y de biotecnología están ampliando sus productos para incluir moléculas pequeñas, productos biológicos y terapias avanzadas, que requieren mayores pruebas de materias primas, controles durante el proceso, microbiología, estudios de estabilidad, validación y asistencia para la liberación de lotes. Un aumento en los programas de desarrollo también aumenta la demanda de métodos analíticos que cumplan con las GMP, sistemas de documentación mejorados y controles de cumplimiento más estrictos a medida que los candidatos pasan del desarrollo a la fabricación clínica y comercial. Esto aumenta directamente la necesidad de instrumentos de control de calidad, consumibles, software de calidad y servicios de pruebas/cumplimiento subcontratados.
- Por ejemplo, en abril de 2025, Novartis anunció planes de invertir 23.000 millones de dólares en cinco años para ampliar su huella de fabricación e I+D en Estados Unidos, incluidas 10 instalaciones, de las cuales 7 son nuevas.
RESTRICCIONES DEL MERCADO
Requisitos regulatorios estrictos para limitar el crecimiento del mercado
Los estrictos requisitos regulatorios son una restricción clave del mercado, ya que aumentan el costo, la complejidad y el tiempo necesario para mantener operaciones que cumplan con las GMP. Los fabricantes de medicamentos deben invertir mucho en sistemas validados, controles de documentación, supervisión de calidad, integridad de datos, monitoreo ambiental, capacitación de empleados y preparación para auditorías para cumplir con la FDA, la EMA y otros estándares regulatorios. Incluso las brechas menores en la supervisión de la unidad de calidad, la validación de la limpieza, el control de la contaminación o la documentación de los lotes pueden generar cartas de advertencia, costos de remediación, retrasos en la liberación del producto o interrupciones en el suministro. Estos requisitos son especialmente onerosos para los fabricantes más pequeños y para las empresas que se expanden hacia productos biológicos, productos estériles u operaciones globales en múltiples sitios. Si bien las regulaciones estrictas respaldan la seguridad de los productos, también aumentan los costos operativos y retrasan la implementación de nuevos procesos, instalaciones y transferencias de productos.
- Por ejemplo, en agosto de 2025, la FDA de EE. UU. emitió una carta de advertencia a Amneal Pharmaceuticals luego de una inspección en marzo de 2025 de sus instalaciones en Gujarat, India. La carta resumió violaciones significativas de CGMP para productos farmacéuticos terminados, ilustrando cómo el incumplimiento puede conducir a acciones regulatorias, cargas de remediación y posibles interrupciones operativas.
OPORTUNIDADES DE MERCADO
Adopción creciente de servicios de control de calidad subcontratados para ofrecer oportunidades de crecimiento del mercado
El uso cada vez mayor de servicios de control de calidad subcontratados presenta una oportunidad importante en el sector de cumplimiento y control de calidad farmacéutica. Las empresas farmacéuticas y de biotecnología están delegando progresivamente tareas de control de calidad a socios especializados para lograr tiempos de respuesta más rápidos, capacidad de laboratorio certificada por GMP y habilidades analíticas mejoradas sin incurrir en gastos de capital internos significativos. Esto está ganando importancia a medida que los productos biológicos, las vacunas y las células yterapias genéticasrequieren pruebas de liberación cada vez más complejas, gestión de la contaminación, verificación de métodos y asistencia para la estabilidad. La subcontratación ayuda a las empresas a manejar volúmenes de producción fluctuantes, aliviando el estrés en los equipos internos de control de calidad y mejorando la flexibilidad durante la ampliación o la producción en múltiples sitios. Además, los proveedores de servicios internacionales pueden facilitar pruebas estandarizadas en varias regiones, lo que resulta beneficioso para las empresas que operan en varios mercados regulatorios.
- Por ejemplo, Eurofins Scientific y Charles River Laboratories son algunas de las empresas que ofrecen servicios de control de calidad.
DESAFÍOS DEL MERCADO
Complejidad de mantener estándares de calidad consistentes en las cadenas de suministro globalesPlantean un desafío destacado para el crecimiento del mercado
El desafío de garantizar estándares de calidad uniformes en todas las cadenas de suministro globales es un tema importante en el mercado de cumplimiento y control de calidad farmacéutica. Las empresas farmacéuticas están obteniendo progresivamente API, excipientes, productos intermedios,materiales de embalajey soporte de fabricación de dosis terminadas de varios países, lo que complica el mantenimiento de una ejecución GMP consistente en todos los sitios y proveedores. Las variaciones en los sistemas de calidad de los proveedores, las metodologías de documentación, la intensidad de las pruebas, las medidas de integridad de los datos y el desarrollo regulatorio pueden generar inconsistencias que aumentan el riesgo de cumplimiento. Este problema se vuelve cada vez más importante cuando las empresas manejan cadenas de suministro extensas y de múltiples capas para productos biológicos, medicamentos estériles o genéricos de gran volumen, donde incluso una deficiencia de calidad menor puede posponer la liberación de lotes o iniciar una solución. También aumenta la necesidad de calificación de proveedores, programas de auditoría, control de contaminación, trazabilidad y sistemas unificados de gestión de calidad en diferentes regiones. En consecuencia, las empresas deben invertir más en supervisión, verificación, soluciones de calidad digital y pruebas de terceros para garantizar que las operaciones globales sigan coordinadas.
- Por ejemplo, en julio de 2025, la OMS señaló que los medicamentos contaminados a menudo surgen de vulnerabilidades sistémicas en la cadena de suministro global de excipientes farmacéuticos.
Análisis de segmentación
Ofreciendo
El amplio uso de instrumentos y consumibles de control de calidad permitió dominar el segmento de productos
En términos de oferta, el mercado se divide en productos, software y servicios. El segmento de productos se divide a su vez en instrumentos y consumibles.
El segmento de productos lideró la cuota de mercado mundial de cumplimiento y control de calidad farmacéutica en 2025. El dominio del segmento se debe a la función vital de los instrumentos y consumibles en el día a día.control de calidad farmaceuticatareas, incluido el análisis de materias primas, evaluaciones en proceso, evaluaciones microbiológicas, evaluaciones de esterilidad, pruebas de estabilidad y liberación de lotes de productos terminados. Además, cada instalación de fabricación regulada necesita un acuerdo de control de calidad tangible, lo que genera gastos constantemente elevados en sistemas de cromatografía, equipos de pruebas microbiológicas, instrumentos de monitoreo, reactivos, medios, filtros y sustancias de referencia.
- Por ejemplo, en mayo de 2024, Sartorius anunció el lanzamiento de su bomba Sterisart Universal de cuarta generación para pruebas de esterilidad. El sistema está diseñado para cumplir con los estrictos estándares de calidad y seguridad de las industrias farmacéutica y biotecnológica, al mismo tiempo que admite documentación compatible con 21 CFR Parte 11 para una mayor integridad de los datos y preparación para auditorías.
Se prevé que el segmento de software aumente con una tasa compuesta anual del 12,03% durante el período previsto.
Para saber cómo nuestro informe puede ayudar a optimizar su negocio, Hable con un analista
Por aplicación
La amplia base de fabricación de fármacos de moléculas pequeñas respaldó el dominio segmentario
Según la aplicación, el mercado se clasifica en medicamentos de molécula pequeña, productos biológicos ybiosimilares, vacunas, terapias celulares y genéticas, entre otros.
El segmento de medicamentos de molécula pequeña representó la participación dominante debido a la amplia capacidad de fabricación mundial de tabletas, cápsulas, inyectables y otros artículos farmacéuticos tradicionales, lo que generó una demanda significativa y continua de pruebas de materias primas, inspecciones en proceso, evaluaciones de disolución, evaluaciones de impurezas, investigación de estabilidad y liberación de lotes de productos terminados. Además, los productos de moléculas pequeñas se fabrican en volúmenes de lotes más grandes y en más ubicaciones que las modalidades avanzadas, lo que garantiza que los gastos en instrumentos de control de calidad, consumibles y sistemas de cumplimiento sigan siendo sólidos. Además, se espera que el segmento tenga una participación del 54,3% en 2026.
- Por ejemplo, en octubre de 2025, Merck inició la construcción de un Centro de Excelencia farmacéutica valorado en 3.000 millones de dólares en Elkton, Virginia. La compañía afirmó que la expansión incluye inversiones en ingredientes farmacéuticos activos y productos farmacéuticos que respaldan la fabricación y las pruebas de moléculas pequeñas.
Se prevé que el segmento de vacunas aumente con una tasa compuesta anual del 9,22% durante el período previsto.
Por función
La necesidad crítica de verificación de la calidad final antes del lanzamiento comercial permitió que el segmento dominara
Según su función, el mercado se divide en control de calidad de materias primas, control de microbiología y contaminación, pruebas de estabilidad y vida útil, control de calidad en proceso, pruebas de productos terminados y liberación de lotes, gestión de cumplimiento normativo, validación y calificación/gestión de sistemas de calidad, y otros.
En 2025, el mercado estaba liderado principalmente por el segmento de pruebas de productos terminados y liberación de lotes y se espera que tenga una participación del 21,3% en 2026. El dominio del segmento se debe a la necesidad de que cada lote farmacéutico debe someterse a controles de especificaciones finales antes del envío, lo que hace que esta función sea esencial tanto en la producción de moléculas pequeñas como de productos biológicos. Además, las pruebas de productos terminados combinan actividades de ensayo, impurezas, disolución, esterilidad, potencia y revisión de documentación, abarcando así una parte importante de los gastos de control de calidad y cumplimiento. Dado que los retrasos durante la fase de lanzamiento de lotes pueden afectar directamente la disponibilidad del producto, el capital de trabajo y el tiempo de comercialización, los fabricantes siguen invirtiendo significativamente en procesos de lanzamiento más rápidos, confiables y mejor conectados. El requisito continuo de validación del producto final y preparación para el lanzamiento refuerza la sólida posición de mercado del segmento.
- Por ejemplo, en mayo de 2025, Veeva destacó la creciente necesidad de optimizar los complejos flujos de trabajo de liberación de lotes y mejorar las decisiones de suministro de productos a través de un enfoque centralizado y automatizado.
Se prevé que el segmento de gestión del cumplimiento normativo aumente con una tasa compuesta anual del 10,84% durante el período previsto.
Por usuario final
Las empresas farmacéuticas y de biotecnología lideraron la demanda debido al alto gasto en control de calidad y cumplimiento normativo
Según el usuario final, el mercado se segmenta enfarmacéuticoy empresas de biotecnología, CRO y CDMO, y otros.
El segmento de empresas farmacéuticas y de biotecnología dominó el mercado en 2025, ya que poseen directamente las responsabilidades de desarrollo, fabricación, liberación de lotes y cumplimiento normativo de medicamentos. Además, son los principales compradores de instrumentos de control de calidad, consumibles, software de calidad, sistemas de microbiología, herramientas de validación y servicios de cumplimiento necesarios para mantener los estándares GMP en las redes de fabricación internas. Dado que gestionan la calidad del producto desde las pruebas de la materia prima hasta el lanzamiento del producto terminado, su gasto sigue siendo mayor que el de los actores subcontratados en términos de valor general. Además, se espera que el segmento tenga una participación del 71,4% en 2026.
- Por ejemplo, en julio de 2024, Biogen anunció una inversión de 2.000 millones de dólares en fabricación en Carolina del Norte. La empresa afirmó que sus campus cuentan con sofisticados laboratorios de control de calidad para garantizar la seguridad, eficacia y pureza de los medicamentos.
Además, se prevé que las CRO/CDMO experimenten una tasa de crecimiento del 10,95% durante el período previsto.
Perspectivas regionales del mercado de cumplimiento y control de calidad farmacéutica
Por geografía, el mercado se divide en América Latina, Asia Pacífico, Europa, América del Norte y Medio Oriente y África.
América del norte
North America Pharma Quality Control and Compliance Market Size, 2025 (USD Billion)
Para obtener más información sobre el análisis regional de este mercado, Descargar muestra gratuita
América del Norte ocupó la mayor parte del mercado y alcanzó 3.880 millones de dólares en 2024 y mantuvo su dominio en 2025 con 4.130 millones de dólares. América del Norte se está expandiendo debido a su sólida base en la producción farmacéutica, biotecnológica y de terapias avanzadas. El área asigna importantes fondos para el cumplimiento de GMP, validación, garantía de esterilidad, pruebas de liberación de lotes y sistemas de calidad digitales.
Mercado de cumplimiento y control de calidad farmacéutica de EE. UU.
El mercado estadounidense lideró a América del Norte y se prevé que alcanzará aproximadamente 3.850 millones de dólares en 2026, lo que representa alrededor del 33,3% del mercado mundial.
Europa
Se estima que el mercado europeo crecerá a una tasa compuesta anual del 7,90% durante el período previsto, impulsado por una amplia red de fabricación farmacéutica, una sólida base de producción de vacunas y productos biológicos y un entorno GMP bien establecido. La región también se beneficia de una fuerte presencia de CDMO, que respalda los servicios de cumplimiento y pruebas de control de calidad subcontratados.
Mercado de cumplimiento y control de calidad farmacéutica del Reino Unido
Se estima que el mercado del Reino Unido alcanzará alrededor de 480 millones de dólares estadounidenses para 2026, lo que representa aproximadamente el 4,2 % de los ingresos mundiales.
Mercado de cumplimiento y control de calidad farmacéutica de Alemania
Se prevé que Alemania alcanzará aproximadamente 670 millones de dólares en 2026, lo que equivale a alrededor del 5,8% de las ventas mundiales.
Asia Pacífico
Se espera que el tamaño del mercado de Asia Pacífico alcance una valoración de 2.760 millones de dólares en 2026 y es la región de más rápido crecimiento debido al rápido aumento de las capacidades de producción farmacéutica en China e India. El área está experimentando una mayor inversión en laboratorios de control de calidad, pruebas microbiológicas, gestión de la contaminación y sistemas de fabricación que cumplen con las GMP para facilitar tanto el suministro local como los mercados de exportación.
Mercado de cumplimiento y control de calidad farmacéutica de Japón
En 2026, se prevé que Japón alcance los 560 millones de dólares, lo que representa aproximadamente el 4,9% de los ingresos mundiales.
Mercado de cumplimiento y control de calidad farmacéutica de China
Se prevé que el mercado de China alcance alrededor de 890 millones de dólares en 2026, lo que representa aproximadamente el 7,7% de las ventas mundiales.
Mercado de cumplimiento y control de calidad farmacéutica de la India
Se estima que en 2026, la India alcanzará 520 millones de dólares, lo que representa aproximadamente el 4,5% de los ingresos mundiales.
América Latina y Medio Oriente y África
Se prevé que el crecimiento en América Latina, Medio Oriente y África será moderado en los próximos años, impulsado por una mayor inversión en la fabricación farmacéutica local, un mayor enfoque en el cumplimiento normativo y esfuerzos para reducir la dependencia de los medicamentos importados. El tamaño del mercado de la región se estima en alrededor de 750 millones de dólares para 2026.
Se prevé que el mercado del CCG alcance aproximadamente 200 millones de dólares en 2026, lo que representa alrededor del 1,8% de los ingresos mundiales.
PAISAJE COMPETITIVO
Actores clave de la industria
Portafolios de control de calidad integrados y capacidades de cumplimiento digital en expansión para respaldar la posición de los jugadores en el mercado
El mercado global refleja un panorama competitivo semifragmentado, formado por Thermo Fisher Scientific Inc., Agilent Technologies Inc., Waters Corporation, Sartorius AG y otras empresas importantes que también representan ingresos importantes. La considerable presencia de mercado de estas empresas está respaldada por sus amplias carteras y su fuerte presencia geográfica. Además, estos actores se están centrando en ecosistemas de calidad integrados que conectan flujos de trabajo de control de calidad, capacitación, validación, liberación de lotes y cumplimiento, lo que se espera que fortalezca su posición competitiva.
Otros participantes importantes incluyen Charles River Laboratories, Eurofins Scientific, LabVantage Solutions Inc. y LabWare. Se prevé que estas empresas se centrarán en la mejora de productos, productos integrados y lanzamientos de nuevos productos para elevar su posición en el mercado.
- Por ejemplo, en agosto de 2024, Veeva Systems anunció un impulso creciente para Veeva Vault LIMS, una solución de control de calidad basada en la nube unificada con Veeva Vault Quality. La compañía afirmó que esta configuración ayuda a las empresas de ciencias biológicas a conectar los procesos de control de calidad y calidad, reducir la documentación en papel y respaldar decisiones de liberación de lotes más informadas.
LISTA DE EMPRESAS CLAVE DE CONTROL DE CALIDAD Y CUMPLIMIENTO FARMACÉUTICO
- Termo Fisher Scientific Inc.(A NOSOTROS.)
- Tecnologías Agilent, Inc.(A NOSOTROS.)
- Corporación de aguas(A NOSOTROS.)
- Sistemas Veeva(A NOSOTROS.)
- Honeywell International Inc. (EE. UU.)
- Sartorius AG (Alemania)
- Laboratorios Charles River (EE. UU.)
- Eurofins Scientific (Luxemburgo)
- LabVantage Solutions Inc. (EE. UU.)
- LabWare (EE. UU.)
DESARROLLOS CLAVE DE LA INDUSTRIA
- Enero de 2026:Charles River reveló su intención de adquirir PathoQuest. Charles River afirmó que el acuerdo mejoraría sus capacidades de prueba de productos biológicos al incorporar soluciones de prueba GMP rápidas y avanzadas, como la plataforma de control de calidad iDTECT de PathoQuest para identificar agentes adventicios y caracterizar líneas celulares y vectores virales.
- Mayo de 2025:Waters Corporation anunció que Empower Software ahora admite la adquisición de datos biológicos y el análisis de control de calidad de los instrumentos Wyatt MALS y RI.
- Marzo de 2025:LabVantage lanzó LabVantage 8.9, la última versión de su plataforma LIMS. La actualización está diseñada para mejorar la productividad del laboratorio, garantizar la precisión y el cumplimiento, y simplificar los flujos de trabajo complejos, con automatización adicional y eficiencias impulsadas por la IA relevantes para los entornos de control de calidad regulados.
- Marzo de 2025:LabWare amplió su cartera de SaaS con LabWare ASSURE, junto con LabWare QAQC y LabWare GROW.
- Enero de 2025:Veeva y Zifo revelaron un esfuerzo colaborativo de producto para acelerar la modernización del control de calidad. La integración fusiona Veeva LIMS con la plataforma qcKen de Zifo, lo que permite a las empresas importar datos de documentos fuente o diferentes sistemas LIMS, aliviando los desafíos de configuración de datos maestros y acelerando la implementación de LIMS y el despliegue del sitio.
COBERTURA DEL INFORME
El análisis del mercado global de cumplimiento y control de calidad farmacéutica incluye una evaluación exhaustiva del tamaño del mercado y pronósticos para cada segmento destacado en el informe. Ofrece información sobre la dinámica del mercado y las tendencias que se espera que impulsen el mercado durante el período de pronóstico. Proporciona comprensión de factores esenciales, incluido el progreso tecnológico, las innovaciones de productos, el entorno regulatorio y el lanzamiento de nuevos productos. Además, detalla asociaciones, fusiones y adquisiciones, así como desarrollos clave en la industria dentro del mercado. El informe también proporciona un panorama competitivo en profundidad, que incluye información sobre la cuota de mercado y los perfiles de los actores activos clave.
Solicitud de personalización para obtener un conocimiento amplio del mercado.
Alcance y segmentación del informe
| ATRIBUTO | DETALLES |
| Período de estudio | 2021-2034 |
| Año base | 2025 |
| Año estimado | 2026 |
| Período de pronóstico | 2026-2034 |
| Período histórico | 2021-2024 |
| Índice de crecimiento | CAGR del 8,85% entre 2026 y 2034 |
| Unidad | Valor (millones de dólares) |
| Segmentación | Por oferta, aplicación, función, usuario final y región |
| Ofreciendo |
|
| Por aplicación |
|
| Por función |
|
| Por usuario final |
|
| Por región |
|
Preguntas frecuentes
Según Fortune Business Insights, el valor del mercado global se situó en 10.790 millones de dólares en 2025 y se prevé que alcance los 22.820 millones de dólares en 2034.
En 2025, el valor del mercado de América del Norte ascendía a 4.130 millones de dólares.
Se espera que el mercado muestre una tasa compuesta anual del 8,85% durante el período previsto de 2026-2034.
Al ofrecer, se espera que el segmento de productos lidere el mercado.
La creciente demanda debido a las crecientes actividades de desarrollo de medicamentos, un mayor enfoque en el control de la contaminación y la creciente subcontratación a CRO/CDMO están impulsando principalmente la expansión del mercado.
Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation y Sartorius AG son algunos de los actores destacados del mercado global.
América del Norte dominó el mercado en 2025.
Póngase en contacto con nuestras expertas Habla con un experto
Obtenga un 20% de personalización gratuita
Ampliar la cobertura regional y por país, Análisis de segmentos, Perfiles de empresas, Benchmarking competitivo, e información sobre el usuario final.
Informes relacionados