Endotoxin-Testreagenzien Marktgröße, Anteil und Branchenanalyse, nach Produkttyp (LAL/TAL-Reagenzien, rekombinante Endotoxin-Nachweisreagenzien, Standards und Kontrollen und andere), nach Quelle (natürlich, rekombinant und andere), nach Testmethode (Gelgerinnsel, chromogen, turbidimetrisch, rekombinante Methoden und andere), nach Anwendung (Testen pharmazeutischer Produkte, Biologika und Impfstofftests, Prüfung medizinischer Geräte, Prüfung von Rohstoffen, Prüfung von Wasser- und Prozessproben), nach Endbenutzern (Pharma- und Biotechnologieunternehmen, Hersteller medizinischer Geräte, CROs und
Marktgröße und Zukunftsaussichten für Endotoxin-Testreagenzien
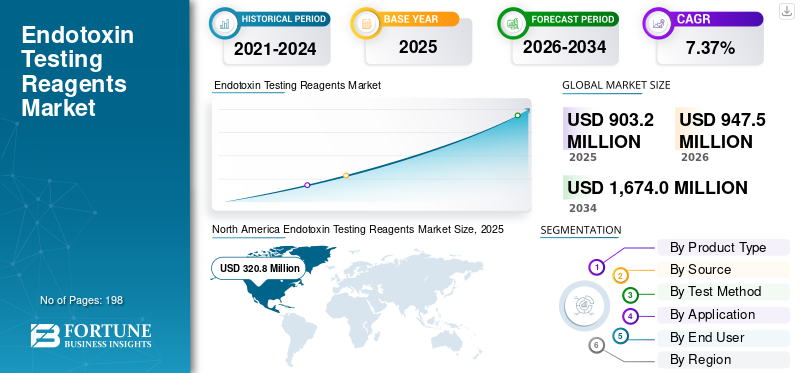
Die weltweite Marktgröße für Endotoxin-Testreagenzien wurde im Jahr 2025 auf 903,2 Millionen US-Dollar geschätzt. Der Markt soll von 947,5 Millionen US-Dollar im Jahr 2026 auf 1.674,0 Millionen US-Dollar im Jahr 2034 wachsen und im Prognosezeitraum eine jährliche Wachstumsrate von 7,37 % aufweisen. Nordamerika dominierte den Markt für Endotoxin-Testreagenzien mit einem Marktanteil von 57,66 % im Jahr 2025.
Reagenzien für Endotoxintests werden in Qualitätskontrollprozessen verwendet, um bakterielle Endotoxine in verschiedenen Proben zu identifizieren und zu messen. Das Marktwachstum wird durch die anhaltende Ausweitung der Produktion von Biologika und sterilen Injektionsmitteln, die zunehmende Bedeutung der Kontaminationskontrolle in der regulierten Fertigung und den zunehmenden Übergang von traditionellen Lysat-basierten Techniken zu rekombinanten Endotoxin-Nachweismitteln vorangetrieben. Auch die globale Marktnachfrage steigt, da Hersteller ihre Qualitätssicherungsmaßnahmen durch Chargenfreigabetests, In-Prozess-Überwachung und Rohstoffqualifizierung verbessern, um die Produktsicherheit, Compliance und Fertigungszuverlässigkeit zu erhöhen.
Zu den wichtigsten Marktteilnehmern zählen Charles River Laboratories, Lonza, Associates of Cape Cod und bioMérieux. Diese Firmen konzentrieren sich auf Assay-Empfindlichkeit, regulatorische Standards, Arbeitsablaufeffizienz und die Fähigkeit, Qualitätskontrollumgebungen für Arzneimittel, Biologika, Impfstoffe und medizinische Geräte zu unterstützen.
Laden Sie ein kostenloses Muster herunter um mehr über diesen Bericht zu erfahren.
ENDOTOXIN-TESTREAGENZIEN MARKTTRENDS
Der Aufstieg tierversuchsfreier Alternativen ist ein bedeutender Trend, der auf dem Weltmarkt zu beobachten ist
Das Aufkommen tierfreier Alternativen ist ein bedeutender Trend auf dem Markt, da pharmazeutische undmedizinisches GerätHersteller suchen zunehmend nach Möglichkeiten, ihre Abhängigkeit von Lysat aus Pfeilschwanzkrebsen zu verringern und gleichzeitig die Empfindlichkeit, Konsistenz und Einhaltung gesetzlicher Vorschriften sicherzustellen. Dieser Übergang erleichtert den schnelleren Einsatz rekombinanter Endotoxin-Nachweisreagenzien, insbesondere in hochwertigen Biologika, Impfstoffen und sterilen Produktionsprozessen. Auch Methoden ohne Einsatz von Tieren erfreuen sich zunehmender Beliebtheit, da sie Unternehmen dabei unterstützen, ihre Nachhaltigkeitsziele zu verbessern, die Versorgungsstabilität zu erhöhen und die mit Reagenzien natürlichen Ursprungs verbundenen Schwankungen zu minimieren. Folglich wandeln sich rekombinante Tests von einer Entwicklungsalternative zu einem kommerziell bedeutenderen Technologiesektor in weltweiten QC-Labors. Diese Faktoren unterstützen das allgemeine Wachstum des globalen Marktes für Endotoxin-Testreagenzien.
- Beispielsweise brachten die Charles River Laboratories im Januar 2024 die Endosafe Trillium rCR-Kartuschen als ersten tierfreien Schnelltest auf bakterielle Endotoxine auf den Markt und kombinierten ihre Kartuschenplattform mit rekombinanter Kaskadenreagenztechnologie, um eine nicht tierische Alternative für Endotoxintests bereitzustellen.
MARKTDYNAMIK
MARKTREIBER
Laden Sie ein kostenloses Muster herunter um mehr über diesen Bericht zu erfahren.
Der kontinuierliche Ausbau der Biologika- und sterilen Injektionsherstellung treibt das Marktwachstum voran
Der kontinuierliche Ausbau der Herstellung von Biologika und sterilen Injektionsmitteln ist ein wichtiger Markttreiber, da mit jeder Erhöhung der Produktionskapazität eine größere Nachfrage nach Chargenfreigabetests, prozessbegleitender Qualitätskontrolle, Rohstoffscreening und Wasser-/Prozessprobenüberwachung entsteht. Biologika, Impfstoffe und sterile Injektionspräparate erfordern eine strenge Kontaminationskontrolle. Wenn Hersteller also neue Linien hinzufügen und ihre Anlagen erweitern, steigt der Reagenzienverbrauch zusammen mit dem Testvolumen. Dies ist besonders wichtig in regulierten Produktionsumgebungen, in denen Endotoxintests eine routinemäßige Sicherheitsanforderung sind, bevor Produkte in der Produktion oder Freigabe weitergeführt werden können. Der Treiber wird immer stärker, da Unternehmen in größere Biologika-Netzwerke, fortschrittlichere sterile Produktionsstätten und höherwertige injizierbare Therapien investieren. Dadurch profitiert der Markt von einer höheren Produktionsleistung und häufigeren, komplexeren QC-Arbeitsabläufen an globalen Produktionsstandorten. All diese Faktoren treiben in ihrer Summe das Gesamtmarktwachstum voran.
- Beispielsweise kündigte AstraZeneca im November 2025 an, dass es 2 Milliarden US-Dollar investieren werde, um seine Produktionsstandorte in Maryland zu erweitern, einschließlich einer erheblichen Erweiterung seiner Biologika-Produktionsanlage in Frederick und einer neuen Anlage in Gaithersburg für die klinische Versorgung innovativer Moleküle.
MARKTBEGRENZUNGEN
Hohe Kosten für fortschrittliche Reagenzien schränken das Marktwachstum ein
Die hohen Kosten für fortschrittliche Reagenzien stellen eine erhebliche Marktbeschränkung dar, da rekombinante Endotoxin-Nachweisreagenzien und schnelle Systeme auf Kartuschenbasis häufig mehr kosten als zahlreiche herkömmliche Techniken auf Lysatbasis. Dies erschwert die Einführung für kleine und mittlere Hersteller, Auftragslabore und preisbewusste Benutzer, insbesondere in Entwicklungsmärkten, in denen die Testfinanzierung stärker eingeschränkt ist. Die erhöhten Kosten sind auf das Assay-Kit, Validierungsaufgaben, Änderungen im Arbeitsablauf und manchmal den Bedarf an Spezialinstrumenten zurückzuführen. Folglich verwenden zahlreiche Labore trotz ihres Interesses an der Einführung neuerer, tierversuchsfreier oder schnellerer Technologien weiterhin traditionelle LAL/TAL-Methoden. Dies behindert die Geschwindigkeit des Übergangs zu Premiumprodukten und schränkt das Umsatzwachstum in preissensiblen Segmenten ein.
- Beispielsweise listete Fisher Scientific am 18. März 2026 die Endosafe Compendial LAL-Kartuschen von Charles River für 531,60 USD für 10 Tests (ca. 53,16 USD pro Test) und das chromogene Endpunkt-Kit von Charles River für 937,62 USD für 140 Tests auf. Diese Preise verdeutlichen, dass fortschrittliche und schnelle Endotoxin-Testlösungen eine erhebliche Kostenbelastung mit sich bringen können.
MARKTCHANCEN
Zunehmende Verlagerung von herkömmlichen Lysat-basierten Methoden hin zu rekombinanten Reagenzien bietet Marktwachstumschancen
Der Übergang von traditionellen lysatbasierten Techniken zu rekombinanten Reagenzien schafft ein erhebliches Marktpotenzial, und zwar in zahlreichen Größenordnungenpharmazeutischund Biotech-Unternehmen suchen nach Endotoxin-Testlösungen, die eine verbesserte Chargenkonsistenz, eine höhere Lieferzuverlässigkeit und eine geringere Abhängigkeit von Materialien aus Pfeilschwanzkrebsen bieten. Dieser Übergang schafft neue Wachstumschancen für Anbieter, die validierte rekombinante Assays, automatisierte Systeme und Workflow-kompatible Lösungen für reguläre QC-Anwendungen liefern können. Es ermöglicht auch Premium-Preisgestaltungsmöglichkeiten; da rekombinante Techniken zunehmend als wertvollere Optionen und nicht nur als Ersatz angesehen werden. Mit der zunehmenden Akzeptanz rekombinanter Tests durch Regulierungsbehörden und die Industrie haben Anbieter eine größere Chance, alte LAL/TAL-Anwender in Biologika, Impfstoffe, sterile Injektionspräparate und medizinische Geräte umzustellen. Dieser Trend ist in umfangreichen Produktionsumgebungen von Bedeutung, in denen Assay-Zuverlässigkeit, Skalierbarkeit und Nachhaltigkeit zunehmend entscheidende Kaufaspekte darstellen. All diese Faktoren würden das Marktwachstum in den kommenden Jahren vorantreiben.
- Beispielsweise gab Lonza im September 2024 bekannt, dass es mit der Erweiterung seiner Produktionsanlage für Endotoxin-Assays in Walkersville, Maryland, begonnen hat. Das Unternehmen gab an, dass mit der Erweiterung die wachsende Nachfrage nach Endotoxin-Testprodukten gedeckt werden soll, was die Annahme stützt, dass das Interesse an fortschrittlichen Endotoxin-Testmethoden steigt.
HERAUSFORDERUNGEN DES MARKTES
Ethische Bedenken hinsichtlich der Verwendung von Pfeilschwanzkrebsblut bei LAL-TestsStellen Sie eine bedeutende Herausforderung für das Marktwachstum dar
Ethische Probleme im Zusammenhang mit der Verwendung von Pfeilschwanzkrebsblut in LAL-Tests stellen eine erhebliche Herausforderung für den Markt dar, da sie den Druck auf die Hersteller erhöhen, gleichzeitig Patientensicherheit, Einhaltung gesetzlicher Vorschriften und Nachhaltigkeitsanforderungen zu berücksichtigen. Herkömmliche LAL-Tests basieren auf Lysat aus Pfeilschwanzkrebsblut, was Bedenken hinsichtlich der anhaltenden Abhängigkeit von dieser Ressource für das Wohlergehen und den Tierschutz aufkommen lässt. Dies führt zu Unsicherheit bei Lieferanten, die immer noch in erheblichem Maße auf Reagenzien natürlichen Ursprungs angewiesen sind, insbesondere da immer mehr Käufer und Aufsichtsbehörden auf tierversuchsfreie Alternativen setzen. Es wirkt sich auch auf die langfristige Lieferstrategie, die Produktplatzierung und den Investitionsfokus im gesamten Markt aus. Folglich stehen Unternehmen vor einem herausfordernden Wandel, da traditionelle Techniken weiterhin vorherrschend bleiben, während sich die Vorlieben der Verbraucher langsam in Richtung innovativer Lösungen verlagern. bioMérieux betont, dass die Abhängigkeit des Pharmasektors von LAL ethische Probleme aufwirft, da es von wilden Pfeilschwanzkrebsen stammt, was das Thema für die Branche immer wichtiger macht. Alle Faktoren wirken sich kumulativ auf das Marktwachstum aus.
Segmentierungsanalyse
Nach Produkttyp
Das Segment der LAL/TAL-Reagenzien dominiert aufgrund seiner starken Legacy-Validierung und seines breiten Routineeinsatzes
Hinsichtlich der Produkttypen ist der Markt in LAL/TAL-Reagenzien, rekombinante Endotoxin-Nachweisreagenzien, Standards und Kontrollen und andere unterteilt.
Das Segment LAL/TAL-Reagenzien hatte im Jahr 2025 den größten Marktanteil bei Endotoxin-Testreagenzien. Dies ist auf seinen langjährigen Einsatz in regulierten Endotoxintests und seine breite Akzeptanz bei verschiedenen Probentests zurückzuführen. Diese Reagenzien haben nach wie vor den größten Anteil, da viele Qualitätskontrolllabore bereits über validierte Arbeitsabläufe, geschultes Personal und etablierte SOPs verfügen, die auf herkömmlichen lysatbasierten Methoden basieren. Ihre breite kommerzielle Verfügbarkeit, die Vertrautheit mit routinemäßigen Chargenfreigabetests und der fortgesetzte Einsatz in kostensensiblen und veralteten Fertigungsumgebungen unterstützen die Segmentdominanz zusätzlich. Darüber hinaus bevorzugen viele Hersteller immer noch LAL/TAL-basierte Assays, da der Wechsel zu neueren Methoden oft zusätzliche Validierungsarbeit, Prozessanpassungen und regulatorische Bequemlichkeit erfordert, was die schnelle Einführung verlangsamt und die führende Position des Segments stärkt.
- Beispielsweise gab FUJIFILM Irvine Scientific im Februar 2024 bekannt, dass es wichtige LAL-Produkte von FUJIFILM Wako Chemicals U.S.A. in sein Life-Sciences-Portfolio aufgenommen hat und damit komplette Endotoxin-Testlösungen erweitert, die direkt für Kunden in den USA und Europa verfügbar sind.
Das Segment der rekombinanten Endotoxin-Nachweisreagenzien wird im Prognosezeitraum voraussichtlich mit einer durchschnittlichen jährlichen Wachstumsrate von 12,66 % wachsen.
Erfahren Sie, wie unser Bericht Ihr Geschäft optimieren kann, Sprechen Sie mit einem Analysten
Nach Quelle
Die starke Akzeptanz von Legacy-Lösungen und die breite installierte Basis unterstützten die Dominanz des Natural-Segments
Basierend auf der Quelle wird der Markt in rekombinante, natürliche und andere unterteilt.
Das natürliche Segment eroberte im Jahr 2025 die führende Position auf dem Weltmarkt. Schlüsselfaktoren, einschließlich seiner seit langem etablierten Verwendung bei bakteriellen Endotoxintests und seiner anhaltenden Akzeptanz bei pharmazeutischen Produkten, Biologika, Impfstoffen, medizinischen Geräten und Wasser-/Prozesstests, unterstützen die Dominanz des Segments. Darüber hinaus bevorzugen viele Hersteller immer noch Methoden auf natürlichen Quellen, da die Umstellung auf rekombinante Alternativen häufig eine erneute Validierung, interne Prozessänderungen und zusätzliche behördliche Genehmigungen erfordert, was die Umwandlung verlangsamt und dazu beiträgt, dass natürliche Reagenzien höhere Umsätze erzielen. Darüber hinaus soll das Segment im Jahr 2026 einen Anteil von 69,2 % halten.
- Beispielsweise stellte Associates of Cape Cod im Jahr 2025 in seiner Ergänzung zu Endotoxintests fest, dass die Industrie immer noch zwei Hauptmethoden verwendet: traditionelle LAL-Reagenzien und rekombinante Reagenzien, was die weiterhin zentrale Rolle traditioneller LAL-Produkte aus natürlichen Quellen in der aktuellen Testpraxis hervorhebt.
Es wird erwartet, dass das rekombinante Segment im Prognosezeitraum mit einer CAGR von 12,65 % wachsen wird.
Nach Testmethode
Das chromogene Segment dominiert aufgrund seiner schnellen Quantifizierung und starken routinemäßigen QC-Nutzung
Basierend auf der Testmethode wird der Markt in Gelgerinnsel-, chromogene, turbidimetrische, rekombinante Methoden und andere unterteilt.
Das chromogene Segment dominierte im Jahr 2025 mit dem größten Marktanteil. Dies ist auf seine hohe Empfindlichkeit, seine quantitativen Ergebnisse und seine weit verbreitete Verwendung in Pharmazeutika, Biologika, Impfstoffen und der Prüfung medizinischer Geräte zurückzuführen. Mit diesem Ansatz wird der höchste Prozentsatz aufrechterhalten, da Laboratorien in die Lage versetzt werden, den Endotoxingehalt genau zu bestimmen und so die regelmäßige Qualitätskontrolle und Prüfung zur Chargenfreigabe zu erleichtern. Die schnellere Abwicklung, die größere Kompatibilität mit Arbeitsabläufen mit hohem Durchsatz und die robuste Ausrichtung auf regulierte Fertigungsumgebungen stärken die Marktführerschaft in diesem Segment weiter. Darüber hinaus bevorzugen zahlreiche Endbenutzer chromogene Assays aufgrund ihrer effektiven Kombination aus Präzision, Arbeitsablaufeffizienz und anerkannter Anwendung in Endotoxin-Testprogrammen, was zu einer starken Nachfrage in QC-Laboren weltweit führt. Darüber hinaus soll das Segment im Jahr 2026 einen Anteil von 35,1 % halten.
- Charles River Laboratories ist beispielsweise einer der führenden Anbieter auf dem Markt, der Produkte für chromogene Tests anbietet.
Es wird erwartet, dass das Segment der rekombinanten Methoden im Prognosezeitraum mit einer CAGR von 12,41 % wachsen wird.
Auf Antrag
Starke Anforderungen an die routinemäßige Freigabe und Qualitätskontrolle führten zur Dominanz des Segments der Prüfung pharmazeutischer Produkte
Je nach Anwendung wird der Markt in pharmazeutische Produkttests, Biologika- und Impfstofftests, medizinische Gerätetests, Rohstofftests, Wasser- und Prozessprobentests und andere unterteilt.
Im Jahr 2025 dominierte das Segment der Arzneimittelprüfung den Markt. Dies ist auf die große Menge an sterilen und injizierbaren Medikamenten zurückzuführen, die vor der Verteilung regelmäßig auf Endotoxine getestet werden müssen. Dieses Segment hält seinen größten Anteil, da Pharmahersteller als Routinebestandteil der Qualitätskontroll- und Compliance-Prozesse Endotoxintests an fertigen Produktchargen durchführen. Das ausgedehnte Netzwerk pharmazeutischer Produktionsanlagen, laufende Chargenfreigabepflichten und die verstärkte Betonung der Produktsicherheit stärken die Dominanz des Segments zusätzlich. Darüber hinaus führt das Testen pharmazeutischer Produkte zu einer stetigen Nachfrage nach Reagenzien, da es sich um einen standardmäßigen, häufig verwendeten Prozess in regulierten Produktionsumgebungen handelt, wodurch weltweit ein hohes Testvolumen aufrechterhalten wird. Darüber hinaus soll das Segment im Jahr 2026 einen Anteil von 34,4 % halten.
- Beispielsweise kündigte Medistri im September 2025 die Ausweitung seiner Dienstleistungen für Arzneimittelfläschchen an und erklärte, dass sein GMP-akkreditiertes Labor Tests auf bakterielle Endotoxine durchführen werde, um die Sicherheit von Arzneimittelfläschchen nachzuweisen.
Die Biologika undImpfstoffEs wird erwartet, dass das Testsegment im Prognosezeitraum mit einer CAGR von 9,39 % wachsen wird.
Vom Endbenutzer
Pharma- und Biotechnologieunternehmen führten die Nachfrage an, da sie in der gesamten Fertigung weit verbreitete Qualitätskontrollen einsetzten
Basierend auf dem Endverbraucher ist der Markt in Pharma- und Biotechnologieunternehmen, Hersteller medizinischer Geräte, CROs und CDMOs und andere unterteilt.
Das Segment Pharma- und Biotechnologieunternehmen dominierte den Markt im Jahr 2025. Diese Dominanz wird durch den erheblichen Einsatz von Endotoxin-Testreagenzien für Fertigarzneimittel, Biologika, Impfstoffe, Rohstoffe und Wasser-/Prozessprobenanalysen vorangetrieben. Dieses Segment hält den größten Anteil, da diese Unternehmen die am stärksten regulierten Herstellungs- und Chargenfreigabeprozesse verwalten, was zu einer konstanten, anhaltenden Nachfrage nach Testreagenzien führt. Ihr intensiver Fokus auf Produktsicherheit, GMP-Einhaltung und Kontaminationsprävention stärkt ihre Führungsposition in diesem Marktsegment weiter. Darüber hinaus erhöht die zunehmende Verbreitung von sterilen Injektionspräparaten, Biologika und fortschrittlichen Therapien die Anforderungen an Endotoxintests in internen Qualitätskontrolllabors, wodurch Pharma- und Biotechnologieunternehmen zum primären Endverbrauchersegment werden. Darüber hinaus soll das Segment im Jahr 2026 einen Anteil von 65,4 % halten.
- Beispielsweise kündigte LGM Pharma im November 2024 die Erweiterung seiner analytischen Testdienstleistungen um Endotoxin- und Schnelltests anSterilitätsprüfung, dass diese Dienstleistungen für Pharmaunternehmen, die sterile und injizierbare Produkte entwickeln, von wesentlicher Bedeutung sind.
Darüber hinaus wird prognostiziert, dass CROs/CDMOs im Prognosezeitraum um 7,11 % wachsen werden.
Regionaler Ausblick auf den Markt für Endotoxin-Testreagenzien
Geografisch ist der Markt in Lateinamerika, den asiatisch-pazifischen Raum, Europa, Nordamerika sowie den Nahen Osten und Afrika unterteilt.
Nordamerika
North America Endotoxin Testing Reagents Market Size, 2025 (USD Million)
Um weitere Informationen zur regionalen Analyse dieses Marktes zu erhalten, Laden Sie ein kostenloses Beispiel herunter
Die nordamerikanische Marktgröße erreichte im Jahr 2024 306,1 Millionen US-Dollar und dominierte den Weltmarkt. Im Jahr 2025 behielt der Bereich mit 320,8 Millionen US-Dollar seinen Spitzenanteil. Das Wachstum in Nordamerika wird hauptsächlich durch die starke Produktionsbasis für Biologika und sterile Injektionsmittel in der Region, die hohe Akzeptanz fortschrittlicher QC-Methoden und die frühe Umstellung auf rekombinante Endotoxin-Testreagenzien unterstützt. Die Region profitiert auch von großen Pharma- und Biotech-Investitionen in neue Produktionskapazitäten.
US-Markt für Endotoxin-Testreagenzien
In Nordamerika waren die USA Marktführer und werden im Jahr 2026 voraussichtlich etwa 290,8 Millionen US-Dollar erreichen, was etwa 30,7 % des Weltmarktes entspricht.
Europa
Es wird erwartet, dass die Marktgröße Europas im Prognosezeitraum mit einer jährlichen Wachstumsrate von 6,36 % wachsen wird. Europa wird von seinen Großen angetriebenbiopharmazeutischund Impfstoffherstellungspräsenz, eine starke regulatorische Qualitätskultur und steigende Investitionen in regionale Bioproduktionskapazitäten. Der Markt profitiert auch von der Modernisierung der Endotoxin-Testpraktiken und dem breiteren Interesse an tierversuchsfreien Methoden.
Britischer Markt für Endotoxin-Testreagenzien
Der britische Markt wird im Jahr 2026 auf etwa 32,4 Millionen US-Dollar geschätzt, was etwa 3,4 % des weltweiten Umsatzes entspricht.
Markt für Endotoxin-Testreagenzien in Deutschland
Die Marktgröße in Deutschland wird im Jahr 2026 voraussichtlich etwa 42,6 Millionen US-Dollar erreichen, was etwa 4,5 % des weltweiten Umsatzes entspricht.
Asien-Pazifik
Es wird erwartet, dass die Marktgröße im asiatisch-pazifischen Raum bis 2026 243,0 Millionen US-Dollar erreichen wird. Es wird erwartet, dass die Region aufgrund der schnellen Expansion in der Biologika-, Impfstoff-, Biosimilars- und CDMO-Herstellung sowie Verbesserungen der QC-Infrastruktur in China, Indien, Japan, Südkorea und Südostasien am schnellsten wächst. Die Region profitiert auch von der zunehmenden exportorientierten Pharmaproduktion, was den Bedarf an konformen Endotoxintests erhöht.
Japan-Markt für Endotoxin-Testreagenzien
Der japanische Markt wird im Jahr 2026 auf rund 49,8 Millionen US-Dollar geschätzt, was etwa 5,3 % des weltweiten Umsatzes ausmacht.
Markt für Endotoxin-Testreagenzien in China
Der chinesische Markt wird im Jahr 2026 voraussichtlich einen Umsatz von rund 72,6 Millionen US-Dollar erreichen, was etwa 7,7 % des weltweiten Umsatzes entspricht.
Markt für Endotoxin-Testreagenzien in Indien
Der indische Markt wird im Jahr 2026 auf rund 34,5 Millionen US-Dollar geschätzt, was etwa 3,6 % des weltweiten Umsatzes ausmacht.
Lateinamerika und der Nahe Osten und Afrika
Das Wachstum in den Regionen Lateinamerika und Naher Osten und Afrika wird im Prognosezeitraum voraussichtlich langsamer ausfallen. Der Markt wird durch erhöhte Produktionskapazitäten für Impfstoffe und Arzneimittel, verbesserte Qualitätskontrollsysteme und eine stärkere Einbindung in regionale und globale Biologika-Lieferketten angetrieben. Der lateinamerikanische Markt wird im Jahr 2026 auf rund 68,5 Millionen US-Dollar geschätzt.
In der Region Naher Osten und Afrika wird der GCC-Markt bis 2026 voraussichtlich etwa 23,9 Millionen US-Dollar erreichen, was etwa 2,5 % des weltweiten Umsatzes entspricht.
WETTBEWERBSFÄHIGE LANDSCHAFT
Wichtige Akteure der Branche
Wichtige Akteure konzentrieren sich auf die Erweiterung ihres Reagenzienportfolios und fortschrittliche Endotoxin-Testlösungen, um ihre Marktposition zu stärken
Der Weltmarkt für Endotoxin-Testreagenzien ist halbkonzentriert, wobei Schlüsselunternehmen wie Charles River Laboratories, Lonza, Associates of Cape Cod und bioMérieux einen erheblichen Teil des Marktumsatzes ausmachen. Ziel dieser Firmen ist es, die Optionen für den Nachweis rekombinanter Endotoxine zu verbessern, die traditionellen LAL/TAL-Reagenzsammlungen zu stärken und die Empfindlichkeit, Zuverlässigkeit und Arbeitsablaufeffizienz der Tests zu steigern, um ihre Marktposition zu stärken.
- Im Juni 2025 ging Charles River beispielsweise eine Partnerschaft mit TerraCycle für ein Endosafe-Kartuschenrecyclingprogramm ein. Mit dem Programm können Benutzer der Endosafe BET-Kartuschentechnologie Einwegkartuschen recyceln, die für routinemäßige Wassertests verwendet werden.
Weitere wichtige Teilnehmer sind FUJIFILM Corporation, Merck KGaA, Thermo Fisher Scientific und regionale Lieferanten wie Bioendo. Von diesen Unternehmen wird erwartet, dass sie neuen Produktinnovationen, Portfolioerweiterungen und einer stärkeren Unterstützung regulierter Qualitätskontrollumgebungen Priorität einräumen, um ihre Wettbewerbsposition im Prognosezeitraum zu verbessern.
LISTE DER WICHTIGSTEN ENDOTOXIN-TESTREAGENZIEN, DIE UNTERNEHMEN PROFILIERT HABEN
- Charles River Laboratories(UNS.)
- Lonza(Schweiz)
- BIOMÉRIEUX (Frankreich)
- FUJIFILM Corporation(Japan)
- Merck KGaA(Deutschland)
- Mitarbeiter von Cape Cod, Inc. (USA)
- Thermo Fisher Scientific Inc. (USA)
- InvivoGen (USA)
- Xiamen Bioendo Technology Co., Ltd. (China)
- ACROBiosystems (USA)
WICHTIGE ENTWICKLUNGEN IN DER INDUSTRIE
- Mai 2025:ACC hat eine formelle Stellungnahme zu USP Kapitel <86> und rekombinanten BET-Reagenzien abgegeben. Das Unternehmen sagte, USP <86> sei ein wichtiger Meilenstein für rekombinante Endotoxintests und bekräftigte, dass PyroSmart NextGen das erste kommerziell erhältliche rCR-Reagenz sei.
- August 2024:Associates of Cape Cod (ACC) erklärte, dass die USP-<86>-Genehmigung dazu geeignet sei, eine breitere Einführung von rekombinantem BET zu unterstützen.
- Juni 2024:FUJIFILM Wako hat zwei neue Pyrogen-/Endotoxintests auf den Markt gebracht: LumiMAT und PYROSTAR Neo+. PYROSTAR Neo+ ist ein rekombinantes Reagenz zum Nachweis von bakteriellem Endotoxin.
- Mai 2024:Bioendo stellte auf der CPHI Shanghai 2024 sein Phoenix Intelligent Automatic Endotoxin Detection System vor.
- März 2022:Bioendo stellte sein neues mikrokinetisches chromogenes Endotoxin-Testkit vor. Es handelt sich um ein spezielles Endotoxin-Reagenzienkit, das eine höhere Empfindlichkeit, einen breiteren linearen Bereich und Kompatibilität mit Impfstoffen, Antikörpern und Biologika bietet.
BERICHTSBEREICH
Die globale Marktanalyse für Endotoxin-Testreagenzien umfasst eine gründliche Bewertung der Marktgröße und Prognosen für jedes im Bericht hervorgehobene Segment. Es bietet Einblicke in die Marktdynamik und Trends, die den Markt im Prognosezeitraum voraussichtlich antreiben werden. Es vermittelt Verständnis für wesentliche Faktoren, darunter technologischen Fortschritt, Produktinnovationen, das regulatorische Umfeld und die Einführung neuer Produkte. Darüber hinaus werden Partnerschaften, Fusionen und Übernahmen sowie wichtige Entwicklungen in der Branche auf dem Markt detailliert beschrieben. Der globale Marktprognosebericht bietet außerdem eine detaillierte Wettbewerbslandschaft, einschließlich Informationen zu Marktanteilen und Profilen der wichtigsten aktiven Akteure.
Anfrage zur Anpassung um umfassende Marktkenntnisse zu erlangen.
Berichtsumfang und Segmentierung
| ATTRIBUT | DETAILS |
| Studienzeit | 2021-2034 |
| Basisjahr | 2025 |
| Geschätztes Jahr | 2026 |
| Prognosezeitraum | 2026-2034 |
| Historische Periode | 2021-2024 |
| Wachstumsrate | CAGR von 7,37 % von 2026 bis 2034 |
| Einheit | Wert (in Mio. USD) |
| Segmentierung | Nach Produkttyp, Quelle, Testmethode, Anwendung, Endbenutzer und Region |
| Nach Produkttyp |
|
| Nach Quelle |
|
| Nach Testmethode |
|
| Per Antrag |
|
| Durch Endbenutzer |
|
| Nach Region |
|
Häufig gestellte Fragen
Laut Fortune Business Insights lag der globale Marktwert im Jahr 2025 bei 903,2 Millionen US-Dollar und soll bis 2034 1.674,0 Millionen US-Dollar erreichen.
Im Jahr 2025 lag der nordamerikanische Marktwert bei 320,8 Millionen US-Dollar.
Der Markt wird im Prognosezeitraum voraussichtlich eine CAGR von 7,37 % aufweisen.
Nach Produkttyp waren die LAL/TAL-Reagenzien im Jahr 2025 marktführend.
Die wachsende Nachfrage nach Biologika und strenge regulatorische Anforderungen an die Arzneimittelsicherheit sind die Schlüsselfaktoren für den Markt.
Charles River Laboratories, Lonza, Associates of Cape Cod und bioMérieux gehören zu den führenden Akteuren auf dem Weltmarkt.
Nordamerika dominierte den Markt im Jahr 2025 mit dem größten Anteil.
Nehmen Sie Kontakt mit unseren Experten auf Sprechen Sie mit einem Experte
20% kostenlose Anpassung erhalten
Regionale und länderspezifische Abdeckung erweitern, Segmentanalyse, Unternehmensprofile, Wettbewerbs-Benchmarking, und Endnutzer-Einblicke.
Verwandte Berichte
-
US +1 833 909 2966 (Gebührenfrei)
-
Nehmen Sie Kontakt mit uns auf