Tamanho do mercado de controle de qualidade e conformidade farmacêutica, análise de participação e indústria, por oferta (produtos {instrumentos e consumíveis}, software e serviços), por aplicação (medicamentos de moléculas pequenas, produtos biológicos e biossimilares, vacinas, terapias celulares e gênicas e outros) por função (controle de qualidade de matérias-primas, controle de microbiologia e contaminação, testes de estabilidade e vida útil, controle de qualidade em processo, testes de produtos acabados e liberação de lote, entre outros), Por usuário final (empresas farmacêuticas e de bio
Tamanho do mercado de controle de qualidade e conformidade farmacêutica e perspectivas futuras
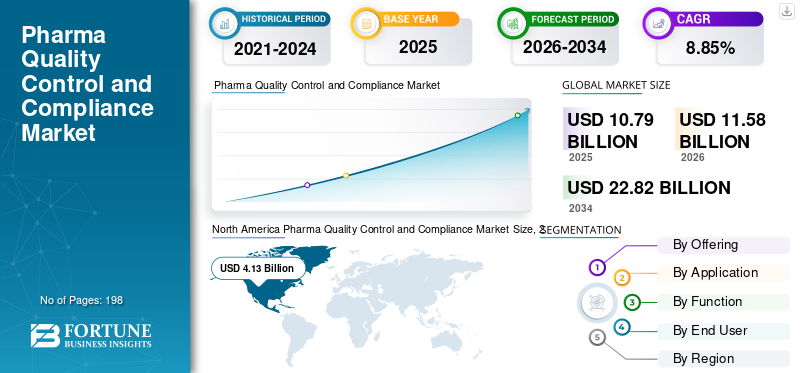
O tamanho global do mercado de controle de qualidade e conformidade farmacêutica foi avaliado em US$ 10,79 bilhões em 2025. O mercado deve crescer de US$ 11,58 bilhões em 2026 para US$ 22,82 bilhões até 2034, exibindo um CAGR de 8,85% durante o período de previsão.
Os sistemas de controle de qualidade e conformidade farmacêutica são utilizados para avaliar a qualidade dos medicamentos, garantir a conformidade com as BPF, supervisionar a documentação regulamentada e auxiliar nas decisões de liberação relacionadas a matérias-primas, lotes em processo, produtos acabados, testes microbiológicos, estabilidade e processos de validação. O mercado está se expandindo à medida que as empresas farmacêuticas e de biotecnologia estão aumentando os investimentos em ferramentas de CQ, consumíveis, sistemas de qualidade digital e testes GMP terceirizados para lidar com a crescente complexidade de fabricação de pequenas moléculas, produtos biológicos,vacinase terapias celulares e genéticas. A procura é ainda reforçada por uma maior ênfase no controlo de contaminação, integridade de dados, eficiência de libertação de lotes, processos de validação e qualificação, juntamente com sistemas de gestão de qualidade baseados na nuvem que melhoram a preparação para auditorias e a adesão regulamentar.
Os principais players que operam no mercado global incluem Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation, Sartorius AG, entre outros. Essas empresas estão se concentrando em avanços tecnológicos em seus produtos, colaborações estratégicas e expansão de portfólio para manter presença no mercado.
Descarregue amostra grátis para saber mais sobre este relatório.
CONTROLE DE QUALIDADE E CONFORMIDADE FARMACÊUTICA TENDÊNCIAS DE MERCADO
A mudança em direção a soluções automatizadas de conformidade é uma tendência significativa observada no mercado global
As empresas farmacêuticas e de biotecnologia estão migrando de processos de qualidade manuais, baseados em papel e desarticulados para sistemas automatizados que podem lidar de forma mais consistente com desvios, CAPA, gerenciamento de documentos, treinamento, revisão de lotes e preparação para auditorias. Esta mudança está ocorrendo à medida que os fabricantes regulamentados exigem tomadas de decisão mais rápidas, melhor rastreabilidade, redução de erros de documentação e maior integridade de dados em operações cada vez mais complexas. Ferramentas automatizadas de conformidade auxiliam as empresas na padronização de procedimentos em vários locais, encurtando a duração dos ciclos de revisão e melhorando a preparação para inspeções e auditorias de BPF. A tendência está se intensificando à medida que aumentam os produtos biológicos, os produtos estéreis e as terapias avançadas, levando a um aumento no volume de eventos de qualidade e documentação de conformidade que precisam ser tratados em tempo real. Consequentemente, as empresas farmacêuticas estão a investir mais recursos em eQMS, LIMS, libertação digital de lotes e plataformas de fluxo de trabalho orientadas por IA que ligam sistemas de qualidade, produção e regulação.
- Por exemplo, em janeiro de 2025, a Honeywell lançou a plataforma TrackWise Life Sciences, que foi projetada para transformar a forma como as organizações de ciências biológicas abordam a fabricação integrada e o gerenciamento da qualidade por meio da transformação digital e da automação avançada.
DINÂMICA DE MERCADO
MOTORIZADORES DE MERCADO
Descarregue amostra grátis para saber mais sobre este relatório.
Aumento da demanda devido ao aumento das atividades de desenvolvimento de medicamentos para impulsionar o crescimento do mercado
A crescente necessidade decorrente do aumento das atividades de desenvolvimento de medicamentos é um fator importante que impulsiona o controle de qualidade farmacêutica e o crescimento do mercado de conformidade. As empresas farmacêuticas e de biotecnologia estão a alargar os seus canais para incluir pequenas moléculas, produtos biológicos e terapias avançadas, que exigem mais testes de matérias-primas, controlos em processo, microbiologia, estudos de estabilidade, validação e assistência na libertação de lotes. Um aumento nos programas de desenvolvimento também aumenta a demanda por métodos analíticos compatíveis com GMP, sistemas de documentação aprimorados e controles de conformidade mais rígidos à medida que os candidatos fazem a transição do desenvolvimento para a fabricação clínica e comercial. Isso aumenta diretamente a necessidade de instrumentos de CQ, consumíveis, software de qualidade e serviços terceirizados de testes/conformidade.
- Por exemplo, em Abril de 2025, a Novartis anunciou planos para investir 23 mil milhões de dólares ao longo de cinco anos para expandir a sua presença na produção e I&D nos EUA, incluindo 10 instalações, das quais 7 são novas.
RESTRIÇÕES DE MERCADO
Requisitos regulatórios rigorosos para limitar o crescimento do mercado
Requisitos regulatórios rigorosos são uma restrição importante do mercado, pois aumentam o custo, a complexidade e o tempo necessário para manter as operações em conformidade com as BPF. Os fabricantes de medicamentos devem investir fortemente em sistemas validados, controlos de documentação, supervisão de qualidade, integridade de dados, monitorização ambiental, formação de funcionários e preparação para auditorias para cumprir a FDA, EMA e outras normas regulamentares. Mesmo pequenas lacunas na supervisão da unidade de qualidade, validação de limpeza, controle de contaminação ou documentação de lote podem gerar cartas de advertência, custos de remediação, atraso na liberação do produto ou interrupção no fornecimento. Esses requisitos são especialmente onerosos para fabricantes menores e para empresas que estão expandindo para produtos biológicos, produtos estéreis ou operações globais em vários locais. Embora regulamentações rigorosas apoiem a segurança dos produtos, elas também aumentam os custos operacionais e retardam a implementação de novos processos, instalações e transferências de produtos.
- Por exemplo, em agosto de 2025, a FDA dos EUA emitiu uma carta de advertência à Amneal Pharmaceuticals após uma inspeção em março de 2025 às suas instalações em Gujarat, na Índia. A carta resumiu violações significativas do CGMP para produtos farmacêuticos acabados, ilustrando como a não conformidade pode levar a ações regulatórias, carga de remediação e potencial interrupção operacional.
OPORTUNIDADES DE MERCADO
Adoção crescente de serviços terceirizados de controle de qualidade para oferecer oportunidades de crescimento de mercado
O uso crescente de serviços terceirizados de controle de qualidade apresenta uma oportunidade significativa no setor de controle de qualidade e conformidade farmacêutica. As empresas farmacêuticas e de biotecnologia estão delegando progressivamente tarefas de CQ a parceiros especializados para alcançar tempos de resposta mais rápidos, capacidade laboratorial certificada por GMP e competências analíticas melhoradas sem incorrer em despesas de capital internas significativas. Isto está ganhando importância à medida que produtos biológicos, vacinas e células eterapias genéticasnecessitam de testes de liberação cada vez mais complexos, gerenciamento de contaminação, verificação de métodos e assistência de estabilidade. A terceirização ajuda as empresas a lidar com volumes de produção flutuantes, aliviando o estresse nas equipes internas de QA/QC e aumentando a flexibilidade durante o escalonamento ou a produção em vários locais. Além disso, os prestadores de serviços internacionais podem facilitar testes padronizados em várias regiões, o que é benéfico para as empresas que operam em vários mercados regulatórios.
- Por exemplo, Eurofins Scientific e Charles River Laboratories são algumas das empresas que oferecem serviços de controle de qualidade.
DESAFIOS DO MERCADO
Complexidade de manter padrões de qualidade consistentes em todas as cadeias de fornecimento globaisRepresenta um desafio proeminente para o crescimento do mercado
O desafio de garantir padrões de qualidade uniformes em todas as cadeias de abastecimento globais é uma questão significativa no mercado farmacêutico de controle de qualidade e conformidade. As empresas farmacêuticas estão progressivamente adquirindo APIs, excipientes, intermediários,materiais de embalageme suporte à fabricação de doses acabadas de vários países, complicando a manutenção de uma execução consistente de GMP em todas as unidades e fornecedores. Variações nos sistemas de qualidade dos fornecedores, metodologias de documentação, intensidade de testes, medidas de integridade de dados e desenvolvimento regulatório podem levar a inconsistências que aumentam o risco de conformidade. Esta questão torna-se cada vez mais significativa quando as empresas lidam com cadeias de abastecimento extensas e multicamadas de produtos biológicos, medicamentos estéreis ou genéricos de grande volume, onde mesmo uma pequena deficiência de qualidade pode adiar a libertação de lotes ou iniciar a remediação. Também aumenta a necessidade de qualificação de fornecedores, programas de auditoria, controle de contaminação, rastreabilidade e sistemas unificados de gestão de qualidade em diferentes regiões. Consequentemente, as empresas precisam de investir mais em supervisão, verificação, soluções de qualidade digital e testes de terceiros para garantir que as operações globais permanecem coordenadas.
- Por exemplo, em Julho de 2025, a OMS observou que os medicamentos contaminados surgem frequentemente de vulnerabilidades sistémicas na cadeia de abastecimento global de excipientes farmacêuticos.
Análise de Segmentação
Ao oferecer
O amplo uso de instrumentos e consumíveis de controle de qualidade permitiu que o segmento de produtos dominasse
Em termos de oferta, o mercado é dividido em produtos, software e serviços. O segmento de produtos é ainda dividido em instrumentos e consumíveis.
O segmento de produtos liderou a participação de mercado global de controle de qualidade e conformidade farmacêutica em 2025. O domínio do segmento se deve à função vital de instrumentos e consumíveis no dia a diacontrole de qualidade farmacêuticatarefas, incluindo análise de matérias-primas, avaliações em processo, avaliações microbiológicas, avaliações de esterilidade, testes de estabilidade e liberação de lotes de produtos acabados. Além disso, cada instalação de produção regulamentada necessita de um acordo de controle de qualidade tangível, levando a despesas consistentemente elevadas com sistemas de cromatografia, equipamentos de testes microbiológicos, instrumentos de monitoramento, reagentes, meios, filtros e substâncias de referência.
- Por exemplo, em maio de 2024, a Sartorius anunciou o lançamento de sua bomba Sterisart Universal de 4ª geração para testes de esterilidade. O sistema foi projetado para atender aos rígidos padrões de qualidade e segurança das indústrias farmacêutica e de biotecnologia, ao mesmo tempo que oferece suporte à documentação compatível com 21 CFR Parte 11 para maior integridade de dados e prontidão para auditoria.
Prevê-se que o segmento de software aumente com um CAGR de 12,03% durante o período de previsão.
Para saber como nosso relatório pode ajudar a otimizar seu negócio, Fale com um analista
Por aplicativo
Ampla base de fabricação de medicamentos de moléculas pequenas apoiou o domínio segmentar
Com base na aplicação, o mercado é classificado em medicamentos de pequenas moléculas, produtos biológicos ebiossimilares, vacinas, terapias celulares e genéticas, entre outros.
O segmento de medicamentos de pequenas moléculas foi responsável pela participação dominante devido à extensa capacidade mundial de fabricação de comprimidos, cápsulas, injetáveis e outros itens farmacêuticos tradicionais, levando a uma demanda significativa e contínua por testes de matérias-primas, inspeções em processo, avaliações de dissolução, avaliações de impurezas, pesquisa de estabilidade e liberação de lotes de produtos acabados. Além disso, os produtos de moléculas pequenas são fabricados em lotes maiores e em mais locais do que as modalidades avançadas, o que garante que os gastos com instrumentos de CQ, consumíveis e sistemas de conformidade permaneçam robustos. Além disso, o segmento deverá deter 54,3% de participação em 2026.
- Por exemplo, em outubro de 2025, a Merck iniciou a construção de um Centro de Excelência farmacêutica de 3,0 mil milhões de dólares em Elkton, Virgínia. A empresa afirmou que a expansão inclui investimento em ingredientes farmacêuticos ativos e medicamentos, apoiando a fabricação e testes de pequenas moléculas.
Prevê-se que o segmento de vacinas aumente com um CAGR de 9,22% durante o período de previsão.
Por função
Necessidade crítica de verificação final da qualidade antes que o lançamento comercial permitisse que o segmento dominasse
Com base na função, o mercado é dividido em controle de qualidade de matérias-primas, microbiologia e controle de contaminação, testes de estabilidade e prazo de validade, controle de qualidade em processo, testes de produtos acabados e liberação de lote, gestão de conformidade regulatória, validação e qualificação/gestão de sistemas de qualidade, entre outros.
Em 2025, o mercado foi liderado principalmente pelo segmento de testes de produtos acabados e liberação de lotes e deverá deter uma participação de 21,3% em 2026. O domínio do segmento decorre da necessidade de que cada lote farmacêutico passe por verificações de especificações finais antes do envio, tornando esta função essencial tanto na produção de pequenas moléculas quanto na produção biológica. Além disso, os testes de produtos acabados combinam atividades de ensaio, impureza, dissolução, esterilidade, potência e revisão de documentação, abrangendo assim uma parcela significativa dos gastos com controle de qualidade e conformidade. Como os atrasos durante a fase de lançamento em lote podem afetar diretamente a disponibilidade do produto, o capital de giro e o tempo de lançamento no mercado, os fabricantes continuam investindo significativamente em processos de lançamento mais rápidos, mais confiáveis e mais bem conectados. A exigência contínua de validação do produto final e preparação para liberação reforça a posição robusta do segmento no mercado.
- Por exemplo, em maio de 2025, Veeva destacou a necessidade crescente de agilizar fluxos de trabalho complexos de liberação de lotes e melhorar as decisões de fornecimento de produtos por meio de uma abordagem centralizada e automatizada.
Prevê-se que o segmento de gestão de conformidade regulatória aumente com um CAGR de 10,84% durante o período de previsão.
Por usuário final
Empresas farmacêuticas e de biotecnologia lideraram a demanda devido aos altos gastos com controle de qualidade e conformidade regulatória
Com base no usuário final, o mercado é segmentado emfarmacêuticoe empresas de biotecnologia, CROs e CDMOs e outros.
O segmento de empresas farmacêuticas e de biotecnologia dominou o mercado em 2025, pois possuem diretamente responsabilidades de desenvolvimento, fabricação, liberação de lotes e conformidade regulatória de medicamentos. Além disso, são os principais compradores de instrumentos de CQ, consumíveis, software de qualidade, sistemas de microbiologia, ferramentas de validação e serviços de conformidade necessários para manter os padrões GMP em redes internas de produção. Como gerenciam a qualidade do produto, desde o teste da matéria-prima até o lançamento do produto acabado, seus gastos permanecem maiores do que os dos players terceirizados em termos de valor geral. Além disso, o segmento deverá deter 71,4% de participação em 2026.
- Por exemplo, em julho de 2024, a Biogen anunciou um investimento industrial de 2 mil milhões de dólares na Carolina do Norte. A empresa afirmou que seus campi contam com sofisticados laboratórios de controle de qualidade para garantir a segurança, eficácia e pureza dos medicamentos.
Além disso, projeta-se que os CROs/CDMOs testemunhem uma taxa de crescimento de 10,95% durante o período de previsão.
Perspectiva regional do mercado de controle de qualidade e conformidade farmacêutica
Por geografia, o mercado está dividido em América Latina, Ásia-Pacífico, Europa, América do Norte e Oriente Médio e África.
América do Norte
North America Pharma Quality Control and Compliance Market Size, 2025 (USD Billion)
Para obter mais informações sobre a análise regional deste mercado, Descarregue amostra grátis
A América do Norte detinha a maior fatia do mercado e atingiu US$ 3,88 bilhões em 2024 e manteve seu domínio em 2025 com US$ 4,13 bilhões. A América do Norte está se expandindo devido à sua base sólida na produção farmacêutica, de biotecnologia e de terapias avançadas. A área aloca fundos significativos para conformidade com BPF, validação, garantia de esterilidade, testes de liberação de lotes e sistemas de qualidade digital.
Mercado de Controle de Qualidade e Conformidade Farmacêutica dos EUA
O mercado dos EUA liderou a América do Norte e está projetado em aproximadamente US$ 3,85 bilhões em 2026, representando cerca de 33,3% do mercado global.
Europa
Estima-se que o mercado europeu cresça a um CAGR de 7,90% durante o período de previsão, alimentado por uma ampla rede de produção farmacêutica, uma forte base de produção de produtos biológicos e de vacinas e um ambiente de GMP bem estabelecido. A região também beneficia da forte presença do CDMO, que apoia testes de CQ terceirizados e serviços de conformidade.
Mercado farmacêutico de controle de qualidade e conformidade do Reino Unido
O mercado do Reino Unido está estimado em cerca de 0,48 mil milhões de dólares para 2026, representando cerca de 4,2% das receitas globais.
Mercado Alemão de Controle de Qualidade e Conformidade Farmacêutica
A Alemanha deverá atingir aproximadamente 0,67 mil milhões de dólares em 2026, o equivalente a cerca de 5,8% das vendas globais.
Ásia-Pacífico
Espera-se que o tamanho do mercado da Ásia-Pacífico atinja uma avaliação de 2,76 mil milhões de dólares em 2026 e é a região que mais cresce devido ao rápido aumento das capacidades de produção farmacêutica na China e na Índia. A área está a registar um aumento do investimento em laboratórios de CQ, testes microbiológicos, gestão de contaminação e sistemas de fabrico em conformidade com as BPF para facilitar tanto o abastecimento local como os mercados de exportação.
Mercado Japonês de Controle de Qualidade e Conformidade Farmacêutica
Em 2026, o Japão deverá atingir 0,56 mil milhões de dólares, representando cerca de 4,9% das receitas globais.
Mercado farmacêutico de controle de qualidade e conformidade da China
O mercado da China deverá atingir cerca de 0,89 mil milhões de dólares em 2026, representando cerca de 7,7% das vendas globais.
Mercado indiano de controle de qualidade e conformidade farmacêutica
Em 2026, estima-se que a Índia alcance 0,52 mil milhões de dólares, representando cerca de 4,5% das receitas globais.
América Latina e Oriente Médio e África
Prevê-se que o crescimento na América Latina, no Médio Oriente e em África seja moderado nos próximos anos, impulsionado pelo aumento do investimento na produção farmacêutica local, pelo aumento do foco na conformidade regulamentar e pelos esforços para reduzir a dependência de medicamentos importados. O tamanho do mercado da região é estimado em cerca de 0,75 mil milhões de dólares para 2026.
O mercado GCC deverá atingir aproximadamente 0,20 mil milhões de dólares em 2026, representando cerca de 1,8% das receitas mundiais.
CENÁRIO COMPETITIVO
Principais participantes da indústria
Portfólios de controle de qualidade integrados e capacidades de conformidade digital em expansão para apoiar a posição dos players no mercado
O mercado global reflete um cenário competitivo semifragmentado, composto pela Thermo Fisher Scientific Inc., Agilent Technologies Inc., Waters Corporation, Sartorius AG e outras grandes empresas que também representam uma receita significativa. A considerável presença de mercado destas empresas é apoiada pelos seus amplos portfólios e forte presença geográfica. Além disso, esses participantes estão se concentrando em ecossistemas de qualidade integrados que conectam fluxos de trabalho de controle de qualidade, controle de qualidade, treinamento, validação, liberação de lotes e conformidade, o que deverá fortalecer sua posição competitiva.
Outros participantes importantes incluem Charles River Laboratories, Eurofins Scientific, LabVantage Solutions Inc. e LabWare. Prevê-se que essas empresas se concentrem na melhoria de produtos, na integração de produtos e no lançamento de novos produtos para elevar sua posição no mercado.
- Por exemplo, em agosto de 2024, a Veeva Systems anunciou um impulso crescente para o Veeva Vault LIMS, uma solução de controle de qualidade baseada em nuvem unificada com o Veeva Vault Quality. A empresa afirmou que esta configuração ajuda as empresas de ciências biológicas a conectar processos de controle de qualidade e controle de qualidade, reduzir a documentação em papel e apoiar decisões de liberação de lote mais informadas.
LISTA DAS PRINCIPAIS EMPRESAS DE CONTROLE DE QUALIDADE E CONFORMIDADE FARMACÊUTICA
- Termo Fisher Scientific Inc.(NÓS.)
- Agilent Technologies, Inc.(NÓS.)
- Corporação Águas(NÓS.)
- Veeva Sistemas(NÓS.)
- Honeywell International Inc. (EUA)
- Sartorius AG (Alemanha)
- Laboratórios Charles River (EUA)
- Eurofins Scientific (Luxemburgo)
- LabVantage Solutions Inc. (EUA)
- LabWare (EUA)
PRINCIPAIS DESENVOLVIMENTOS DA INDÚSTRIA
- Janeiro de 2026:Charles River revelou sua intenção de adquirir a PathoQuest. Charles River afirmou que o acordo melhoraria suas capacidades de testes biológicos ao incorporar soluções rápidas e avançadas de testes de GMP, como a plataforma de controle de qualidade iDTECT da PathoQuest para identificar agentes adventícios e caracterizar linhas celulares e vetores virais.
- Maio de 2025:A Waters Corporation anunciou que a Empower Software agora suporta aquisição de dados biológicos e análise de controle de qualidade de instrumentos Wyatt MALS e RI.
- Março de 2025:LabVantage lançou o LabVantage 8.9, a versão mais recente de sua plataforma LIMS. A atualização foi projetada para melhorar a produtividade do laboratório, garantir precisão e conformidade e simplificar fluxos de trabalho complexos, com automação adicional e eficiências orientadas por IA relevantes para ambientes de controle de qualidade regulamentados.
- Março de 2025:A LabWare expandiu seu portfólio SaaS com LabWare ASSURE, juntamente com LabWare QAQC e LabWare GROW.
- Janeiro de 2025:Veeva e Zifo revelaram um esforço colaborativo de produto para acelerar a modernização do controle de qualidade. A integração funde o Veeva LIMS com a plataforma qcKen da Zifo, permitindo que as empresas importem dados de documentos de origem ou diferentes sistemas LIMS, aliviando os desafios de configuração de dados mestres e acelerando a implementação do LIMS e a implantação no local.
COBERTURA DO RELATÓRIO
A análise global do mercado de controle de qualidade e conformidade farmacêutica inclui uma avaliação completa do tamanho do mercado e das previsões para cada segmento destacado no relatório. Ele oferece insights sobre a dinâmica e as tendências do mercado que deverão impulsionar o mercado durante todo o período de previsão. Fornece compreensão de fatores essenciais, incluindo progresso tecnológico, inovações de produtos, ambiente regulatório e lançamento de novos produtos. Além disso, detalha parcerias, fusões e aquisições, bem como os principais desenvolvimentos do setor no mercado. O relatório também fornece um cenário competitivo aprofundado, incluindo informações sobre participação de mercado e perfis dos principais participantes ativos.
Pedido de Personalização Para obter informações abrangentes sobre o mercado.
Escopo e segmentação do relatório
| ATRIBUTO | DETALHES |
| Período de estudo | 2021-2034 |
| Ano base | 2025 |
| Ano estimado | 2026 |
| Período de previsão | 2026-2034 |
| Período Histórico | 2021-2024 |
| Taxa de crescimento | CAGR de 8,85% de 2026-2034 |
| Unidade | Valor (US$ bilhões) |
| Segmentação | Por oferta, aplicativo, função, usuário final e região |
| Ao oferecer |
|
| Por aplicativo |
|
| Por Função |
|
| Por usuário final |
|
| Por região |
|
Perguntas Frequentes
De acordo com a Fortune Business Insights, o valor do mercado global situou-se em 10,79 mil milhões de dólares em 2025 e deverá atingir 22,82 mil milhões de dólares em 2034.
Em 2025, o valor de mercado da América do Norte era de US$ 4,13 bilhões.
Espera-se que o mercado apresente um CAGR de 8,85% durante o período de previsão de 2026-2034.
Ao oferecer, espera-se que o segmento de produtos lidere o mercado.
O aumento da procura devido às crescentes atividades de desenvolvimento de medicamentos, o maior foco no controlo da contaminação e a crescente terceirização para CROs/CDMOs estão impulsionando principalmente a expansão do mercado.
Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation e Sartorius AG são alguns dos players proeminentes no mercado global.
A América do Norte dominou o mercado em 2025.
Entre em contacto com os nossos especialistas Fale com um especialista
Obtenha 20% de personalização gratuita
Ampliar a cobertura regional e por país, Análise de segmentos, Perfis de empresas, Benchmarking competitivo, e insights sobre o usuário final.
Relatórios relacionados
-
US +1 833 909 2966 (chamada gratuita)
-
Entre em contacto connosco