制药质量控制和合规市场规模、份额和行业分析,按产品(产品{仪器和消耗品}、软件和服务)、按应用(小分子药物、生物制剂和生物仿制药、疫苗、细胞和基因疗法等)按功能(原材料质量控制、微生物学和污染控制、稳定性和保质期测试、过程中质量控制、成品测试和批次发布)等),按最终用户(制药和生物技术公司、CRO 和 CDMO 等)以及区域预测,2026-2034 年
制药质量控制和合规市场规模及未来展望
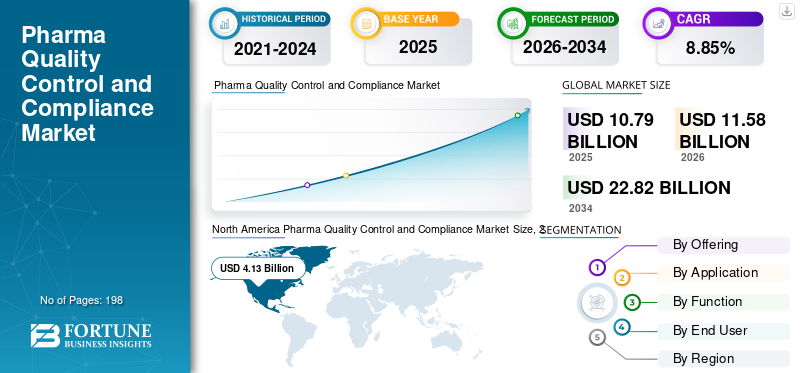
2025年,全球药品质量控制与合规市场规模为107.9亿美元。预计该市场将从2026年的115.8亿美元增长到2034年的228.2亿美元,预测期内复合年增长率为8.85%。
药品质量控制和合规系统用于评估药品质量,确保 GMP 合规性,监督监管文件,并协助与原材料、中间批次、成品、微生物测试、稳定性和验证过程相关的放行决策。随着制药和生物技术公司加大对 QC 工具、耗材、数字质量系统和外包 GMP 测试的投资,以应对小分子、生物制剂、药物等领域日益增加的制造复杂性,该市场正在不断扩大。疫苗,以及细胞和基因疗法。由于越来越重视污染控制、数据完整性、批次放行效率、验证和资格流程,以及增强审计准备和监管遵守的基于云的质量管理系统,进一步推动了这一需求。
全球市场的主要参与者包括 Thermo Fisher Scientific Inc.、Agilent Technologies、Waters Corporation、Sartorius AG 等。 这些公司专注于产品的技术进步、战略合作和产品组合扩展,以维持市场地位。
下载免费样品 了解更多关于本报告的信息。
药品质量控制和合规性 市场趋势
转向自动化合规解决方案是全球市场的一个重要趋势
制药和生物技术公司正在从手动、纸质和脱节的质量流程转向自动化系统,这些系统可以更一致地处理偏差、CAPA、文档管理、培训、批次审查和审计准备。这种变化正在发生,因为受监管的制造商需要在日益复杂的操作中更快地做出决策、提高可追溯性、减少文档错误并增强数据完整性。自动化合规工具可帮助公司标准化不同地点的程序,缩短审查周期持续时间,并加强检查和 GMP 审核的准备工作。随着生物制剂、无菌产品和先进疗法的兴起,这一趋势正在加剧,导致需要实时处理的质量事件和合规文档数量增加。因此,制药公司正在将更多资源投入到 eQMS、LIMS、数字批次放行以及连接质量、制造和监管系统的人工智能驱动的工作流程平台上。
- 例如,2025 年 1 月,霍尼韦尔推出了 TrackWise 生命科学平台,旨在通过数字化转型和先进自动化来改变生命科学组织实现集成制造和质量管理的方式。
市场动态
市场驱动因素
下载免费样品 了解更多关于本报告的信息。
由于药物开发活动增加以促进市场增长,需求不断增长
药物开发活动的增加带来的需求不断增长是推动药品质量控制和合规市场增长的主要因素。制药和生物技术公司正在扩大其产品线,以涵盖小分子、生物制剂和先进疗法,这需要增加对原材料、过程控制、微生物学、稳定性研究、验证和批次发布协助的测试。随着候选药物从开发过渡到临床和商业制造,开发项目的增加也提出了对符合 GMP 的分析方法、增强的文档系统和更严格的合规控制的需求。这直接增加了对质量控制仪器、耗材、质量软件和外包测试/合规服务的需求。
- 例如,2025 年 4 月,诺华宣布计划在五年内投资 230 亿美元,扩大其在美国的制造和研发足迹,包括 10 座设施,其中 7 座是新建的。
市场限制
严格的监管要求限制市场增长
严格的监管要求是一个关键的市场限制,因为它们增加了维持 GMP 合规运营所需的成本、复杂性和时间。药品制造商必须大力投资于经过验证的系统、文件控制、质量监督、数据完整性、环境监测、员工培训和审计准备,以满足 FDA、EMA 和其他监管标准。即使质量部门监督、清洁验证、污染控制或批次文件中的微小差距也可能引发警告信、补救成本、产品发布延迟或供应中断。这些要求对于小型制造商和扩展到生物制品、无菌产品或多地点全球运营的公司来说尤其繁重。虽然严格的法规支持产品安全,但它们也提高了运营成本,并减缓了新工艺、设施和产品转移的实施。
- 例如,2025 年 3 月对 Amneal Pharmaceuticals 位于印度古吉拉特邦的工厂进行检查后,美国 FDA 于 2025 年 8 月向该公司发出了警告信。这封信总结了成品药品严重违反 CGMP 的情况,说明了违规行为如何导致监管行动、补救负担和潜在的运营中断。
市场机会
越来越多地采用外包质量控制服务来提供市场增长机会
越来越多地使用外包质量控制服务为制药质量控制和合规领域带来了重大机遇。制药和生物技术公司逐渐将质量控制任务委托给专业合作伙伴,以实现更快的周转时间、GMP 认证的实验室能力和增强的分析技能,而不会产生大量的内部资本支出。随着生物制剂、疫苗、细胞和药物的应用,这一点变得越来越重要。基因疗法需要日益复杂的放行测试、污染管理、方法验证和稳定性援助。外包可帮助公司应对产量波动、减轻内部 QA/QC 团队的压力,并增强规模化或多地点生产过程中的灵活性。此外,国际服务提供商可以促进各个地区的标准化测试,这有利于企业在多个监管市场中运作。
- 例如,Eurofins Scientific 和 Charles River Laboratories 都是提供质量控制服务的公司。
市场挑战
在全球供应链中保持一致的质量标准的复杂性对市场增长构成突出挑战
确保全球供应链统一质量标准的挑战是药品质量控制和合规市场的一个重大问题。制药公司正在逐步采购原料药、赋形剂、中间体、包装材料以及来自不同国家的成品制剂生产支持,使所有工厂和供应商之间维持一致的 GMP 执行变得复杂化。供应商质量体系、文档方法、测试强度、数据完整性措施和监管制定的变化可能会导致不一致,从而增加合规风险。当企业处理生物制剂、无菌药物或大批量仿制药的广泛、多层供应链时,这个问题变得越来越重要,即使是轻微的质量缺陷也可能会推迟批次放行或启动补救措施。它还提高了不同地区供应商资格、审核计划、污染控制、可追溯性和统一质量管理体系的必要性。因此,企业需要在监督、验证、数字质量解决方案和第三方测试方面进行更多投资,以确保全球运营保持协调。
- 例如,2025 年 7 月,世界卫生组织指出,受污染的药品往往是由于全球药用辅料供应链的系统性漏洞造成的。
细分分析
通过提供
QC 仪器和耗材的广泛使用使产品领域占据主导地位
在产品方面,市场分为产品、软件和服务。产品部分进一步分为仪器和消耗品。
到 2025 年,该产品领域将引领全球制药质量控制和合规市场份额。该领域的主导地位是由于仪器和消耗品在日常中的重要作用药品质量控制任务包括原材料分析、过程评估、微生物评估、无菌评估、稳定性测试和成品批次放行。此外,每个受监管的生产设施都需要有形的质量控制安排,导致色谱系统、微生物测试设备、监测仪器、试剂、介质、过滤器和参考物质的费用持续增加。
- 例如,2024 年 5 月,赛多利斯宣布推出第四代 Sterisart 通用泵,用于无菌测试。该系统旨在满足制药和生物技术行业严格的质量和安全标准,同时还支持 21 CFR Part 11 合规文档,以实现更强的数据完整性和审计准备。
预计软件领域在预测期内将以 12.03% 的复合年增长率增长。
了解我们的报告如何帮助优化您的业务, 与分析师交流
按申请
广泛的小分子药物生产基础支撑了细分领域的主导地位
根据应用,市场分为小分子药物、生物制剂和生物仿制药、疫苗、细胞和基因疗法等。
由于全球范围内片剂、胶囊、注射剂和其他传统药品的广泛生产能力,小分子药物领域占据了主导份额,导致对原材料测试、过程检验、溶出度评估、杂质评估、稳定性研究和成品批量放行的巨大且持续的需求。此外,与先进模式相比,小分子产品在更多地点进行大批量生产,这确保了质量控制仪器、耗材和合规系统的支出保持强劲。此外,该部门预计到 2026 年将持有 54.3% 的份额。
- 例如,2025 年 10 月,默克耗资 30 亿美元的制药卓越中心在弗吉尼亚州埃尔克顿破土动工。该公司表示,扩张包括支持小分子制造和测试的活性药物成分和药品投资。
预计疫苗领域在预测期内将以 9.22% 的复合年增长率增长。
按功能分类
商业发布前对最终质量验证的迫切需求使得该细分市场占据主导地位
根据功能,市场分为原材料质量控制、微生物学和污染控制、稳定性和保质期测试、过程质量控制、成品测试和批次放行、法规遵从性管理、验证和资格/质量体系管理等。
2025年,该市场主要由成品测试和批次放行细分市场主导,预计到2026年将占据21.3%的份额。该细分市场的主导地位源于每个药品批次在装运前必须经过最终规格检查的必要性,使得这一功能在小分子和生物制品生产中都至关重要。此外,成品测试结合了化验、杂质、溶出度、无菌、效力和文件审查活动,从而涵盖了质量控制和合规支出的很大一部分。由于批量发布阶段的延迟会直接影响产品可用性、营运资金和上市时间,因此制造商不断大力投资于更快、更可靠和连接更好的发布流程。对最终产品验证和发布准备的持续要求巩固了该领域稳健的市场地位。
- 例如,2025 年 5 月,Veeva 强调了日益增长的需求,以简化复杂的批量发布工作流程并通过集中和自动化的方法改进产品供应决策。
预计监管合规管理领域在预测期内将以 10.84% 的复合年增长率增长。
按最终用户
由于质量控制和监管合规方面的高支出,制药和生物技术公司引领需求
根据最终用户,市场分为制药和生物技术公司、CRO 和 CDMO 等。
制药和生物技术公司细分市场将在 2025 年占据主导地位,因为它们直接承担药物开发、制造、批次放行和监管合规责任。此外,他们还是内部制造网络维持 GMP 标准所需的 QC 仪器、耗材、质量软件、微生物系统、验证工具和合规服务的主要买家。由于他们管理从原材料测试到成品发布的产品质量,因此从总体价值来看,他们的支出仍然高于外包企业。此外,该部门预计到 2026 年将持有 71.4% 的份额。
- 例如,2024 年 7 月,百健 (Biogen) 宣布在北卡罗来纳州投资 20 亿美元进行制造业投资。该公司表示,其园区拥有先进的质量控制实验室,以确保药品的安全性、有效性和纯度。
此外,预计 CRO/CDMO 在预测期内的增长率将达到 10.95%。
制药质量控制和合规市场区域展望
按地域划分,市场分为拉丁美洲、亚太地区、欧洲、北美、中东和非洲。
北美
North America Pharma Quality Control and Compliance Market Size, 2025 (USD Billion)
获取本市场区域分析的更多信息, 下载免费样品
北美市场占据最大份额,2024 年达到 38.8 亿美元,并在 2025 年以 41.3 亿美元继续保持主导地位。北美因其在制药、生物技术和先进疗法生产方面的坚实基础而不断扩张。该领域为 GMP 合规性、验证、无菌保证、批次放行测试和数字质量系统分配了大量资金。
美国制药质量控制和合规市场
美国市场领先北美,预计2026年约为38.5亿美元,约占全球市场的33.3%。
欧洲
在广泛的药品制造网络、强大的生物制品和疫苗生产基地以及完善的 GMP 环境的推动下,欧洲市场在预测期内预计将以 7.90% 的复合年增长率增长。该地区还受益于强大的 CDMO 存在,支持外包 QC 测试和合规服务。
英国制药质量控制和合规市场
预计 2026 年英国市场规模约为 4.8 亿美元,约占全球收入的 4.2%。
德国制药质量控制和合规市场
预计到 2026 年,德国销售额将达到约 6.7 亿美元,相当于全球销售额的 5.8% 左右。
亚太地区
预计2026年亚太地区市场规模将达到27.6亿美元,由于中国和印度药品生产能力的迅速提升,亚太地区成为增长最快的地区。该地区正在增加对质量控制实验室、微生物检测、污染管理和符合 GMP 的制造系统的投资,以促进当地供应和出口市场。
日本制药质量控制和合规市场
到 2026 年,日本的收入预计将达到 5.6 亿美元,约占全球收入的 4.9%。
中国医药质量控制与合规市场
预计2026年中国市场规模将达到8.9亿美元左右,约占全球销售额的7.7%。
印度制药质量控制和合规市场
2026年,印度预计将实现5.2亿美元的收入,约占全球收入的4.5%。
拉丁美洲、中东和非洲
由于对当地药品制造的投资增加、对监管合规性的日益关注以及努力减少对进口药品的依赖,预计拉丁美洲、中东和非洲的增长在未来几年将温和。 2026 年该地区的市场规模预计约为 7.5 亿美元。
海湾合作委员会市场预计到 2026 年将达到约 2 亿美元,约占全球收入的 1.8%。
竞争格局
主要行业参与者
集成的质量控制产品组合和扩展的数字合规能力以支持参与者的市场地位
全球市场呈现出半分散的竞争格局,包括赛默飞世尔科技公司、安捷伦科技公司、沃特世公司、赛多利斯公司以及其他收入也相当可观的大公司。这些公司广泛的产品组合和强大的地域影响力支撑了其相当大的市场占有率。此外,这些参与者还专注于连接 QA、QC、培训、验证、批次发布和合规工作流程的集成质量生态系统,预计这将增强他们的竞争地位。
其他重要参与者包括 Charles River Laboratories、Eurofins Scientific、LabVantage Solutions Inc. 和 LabWare。预计这些公司将专注于产品改进、集成产品和新产品发布,以提升其市场地位。
- 例如,2024 年 8 月,Veeva Systems 宣布 Veeva Vault LIMS 势头强劲,这是一种与 Veeva Vault Quality 相结合的基于云的质量控制解决方案。该公司表示,这种设置可以帮助生命科学公司连接 QA 和 QC 流程,减少纸质文档,并支持更明智的批次放行决策。
主要药品质量控制和合规公司名单
- 赛默飞世尔科技公司(我们。)
- 安捷伦科技公司(我们。)
- 沃特世公司(我们。)
- Veeva 系统(我们。)
- 霍尼韦尔国际公司(美国)
- 赛多利斯股份公司(德国)
- 查尔斯河实验室(美国)
- Eurofins Scientific(卢森堡)
- LabVantage Solutions Inc.(美国)
- LabWare(美国)
主要行业发展
- 2026 年 1 月:Charles River 透露了收购 PathoQuest 的意向。 Charles River 表示,该协议将通过整合快速、先进的 GMP 测试解决方案来增强其生物制剂测试能力,例如 PathoQuest 的 iDTECT 质量控制平台,用于识别外来因子并表征细胞系和病毒载体。
- 2025 年 5 月:Waters Corporation 宣布 Empower Software 现在支持 Wyatt MALS 和 RI 仪器的生物制剂数据采集和 QC 分析。
- 2025 年 3 月:LabVantage 发布了 LabVantage 8.9,这是其 LIMS 平台的最新版本。该更新旨在提高实验室生产力,确保准确性和合规性,并简化复杂的工作流程,并增加与受监管的质量控制环境相关的自动化和人工智能驱动的效率。
- 2025 年 3 月:LabWare 通过 LabWare ASSURE、LabWare QAQC 和 LabWare GROW 扩展了其 SaaS 产品组合。
- 2025 年 1 月:Veeva 和 Zifo 透露了一项合作产品成果,以加快质量控制的现代化。该集成将 Veeva LIMS 与 Zifo 的 qcKen 平台合并,使公司能够从源文档或不同的 LIMS 系统导入数据,减轻主数据设置挑战并加速 LIMS 实施和现场部署。
报告范围
全球制药质量控制和合规市场分析包括对市场规模的全面评估以及对报告中强调的每个细分市场的预测。它提供了对整个预测期内预计推动市场发展的市场动态和趋势的见解。它提供了对基本因素的理解,包括技术进步、产品创新、监管环境和新产品的推出。此外,它还详细介绍了合作伙伴关系、并购以及市场内行业的关键发展。该报告还提供了深入的竞争格局,包括市场份额信息和主要活跃参与者的概况。
定制请求 获取广泛的市场洞察。
报告范围和细分
| 属性 | 细节 |
| 学习期限 | 2021-2034 |
| 基准年 | 2025年 |
| 预计年份 | 2026年 |
| 预测期 | 2026-2034 |
| 历史时期 | 2021-2024 |
| 增长率 | 2026-2034 年复合年增长率为 8.85% |
| 单元 | 价值(十亿美元) |
| 分割 | 按产品、应用程序、功能、最终用户和区域 |
| 通过提供 |
|
| 按申请 |
|
| 按功能 |
|
| 由最终用户 |
|
| 按地区 |
|
常见问题
根据《财富商业洞察》的数据,2025 年全球市场价值为 107.9 亿美元,预计到 2034 年将达到 228.2 亿美元。
2025年,北美市场价值为41.3亿美元。
预计 2026 年至 2034 年预测期内,市场复合年增长率为 8.85%。
通过提供,该产品领域预计将引领市场。
由于药物开发活动不断增长、对污染控制的更加重视以及对 CRO/CDMO 的外包不断增加,需求不断增加,这主要推动了市场扩张。
Thermo Fisher Scientific Inc.、Agilent Technologies、Waters Corporation 和 Sartorius AG 是全球市场上的一些知名参与者。
2025 年,北美将主导市场。
与我们的专家联系 与专家交谈
相关报道