Tamaño del mercado de biopsia líquida, participación y análisis de la industria, por producto (kits, reactivos e instrumentos), por aplicación (oncología, pruebas prenatales no invasivas (NIPT) y otras), por usuario final (hospitales, laboratorios clínicos y otros) y pronóstico regional, 2026-2034
INFORMACIÓN CLAVE DEL MERCADO
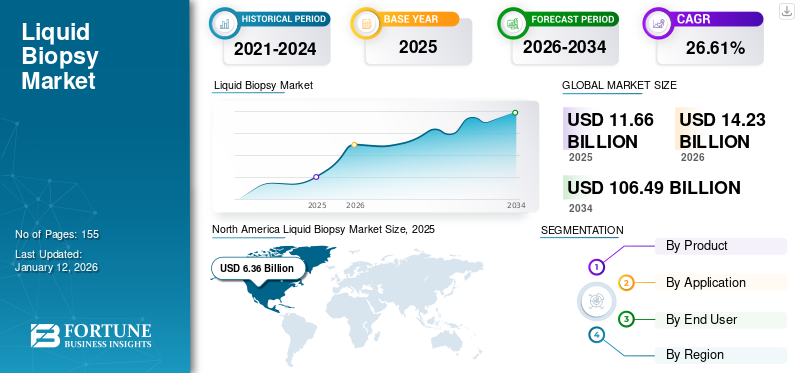
El tamaño del mercado mundial de biopsia líquida se valoró en 11,66 mil millones de dólares en 2025 y se prevé que crezca de 14,23 mil millones de dólares en 2026 a 106,49 mil millones de dólares en 2034, exhibiendo una tasa compuesta anual del 28,61% durante el período previsto. América del Norte dominó el mercado global con una participación del 54,57% en 2025.
El cáncer es uno de los principales contribuyentes a la carga de morbilidad en todo el mundo, con una incidencia cada vez mayor entre la población. Ciertos factores de riesgo ambientales, como la contaminación del aire y los factores de riesgo biológicos, incluido el consumo de tabaco, el tabaquismo y la inactividad física, provocan cáncer y otras enfermedades infecciosas.
- Según datos publicados por el Programa Nacional de Registro de Cáncer del Consejo Indio de Investigación Médica (ICMR), la incidencia estimada de cáncer en la India en 2020 fue de 1,39 millones. La incidencia aumentó de alrededor de 1,42 millones en 2021 a 1,46 millones en 2022.
Por lo tanto, con la creciente prevalencia del cáncer, la demanda de detección temprana y terapias ha aumentado a nivel mundial. Además, la creciente incidencia de anomalías genéticas entre los recién nacidos y fetos de mujeres embarazadas ha llevado a la necesidad de realizar pruebas prenatales entre la población. Además, un aumento en las iniciativas gubernamentales para pruebas de detección públicas para reducir el aumento de enfermedades infecciosas y trastornos crónicos como el cáncer ha llevado a una gran adopción de pruebas de detección no invasivas realizadas con fluidos biológicos como la sangre, el líquido amniótico y el líquido cefalorraquídeo (LCR).
Las pruebas detectan signos de tumores cancerosos, incluidos los circulantes.biomarcadores, ADN libre de células y ADN tumoral circulante (ctDNA), en todos los pacientes con cáncer en etapas de detección o recurrentes. Las agencias reguladoras, como la Administración de Alimentos y Medicamentos (FDA), han aprobado pruebas que pueden detectar cánceres avanzados en un paciente, predecir el pronóstico y ayudar a los proveedores de atención médica a tomar decisiones de tratamiento adicionales. La creciente introducción de pruebas avanzadas para diversas indicaciones y amplios estudios clínicos sobre el desarrollo de nuevos productos impulsarán el crecimiento del mercado de biopsias líquidas durante el período previsto.
El impacto de la pandemia de COVID-19 provocó una disminución del crecimiento del mercado en 2020. La pandemia provocó el aplazamiento y la pérdida de prioridad de pruebas de diagnóstico no esenciales, como la detección del cáncer, por parte de varios organismos de atención sanitaria entre la población. De manera similar, la interrupción causada por la pandemia de COVID-19 en las cadenas de suministro internacionales provocó una escasez notoria de kits y ensayos de diagnóstico del cáncer en todo el mundo.
- Según un artículo publicado por el NCBI en 2021, las pruebas moleculares disminuyeron un 27,0% de 15thmarzo al 15thAbril de 2020, en comparación con el mismo período de 2019. Según estimaciones similares, las pruebas de biopsia líquida para detectar el receptor del factor de crecimiento epidérmico (EGFR) disminuyeron aproximadamente un 67,0 % durante un período de tiempo similar en Italia.
Sin embargo, el levantamiento de las restricciones de bloqueo después de la pandemia y la reanudación de los programas de detección llevaron a un aumento de las pruebas de pronóstico del cáncer. El aumento de la adopción de pruebas caseras y la gran demanda de pruebas oncológicas entre los pacientes impulsaron aún más el crecimiento del mercado.
- Según las estimaciones del informe anual de Guardant Health, Inc. en 2021, las pruebas clínicas de oncología de precisión aumentaron a 87,600 para el año que finalizó en diciembre de 2021 desde 63,254 para el año que finalizó en diciembre de 2020.
Así, el repunte de los casos de detección de cáncer pospandemia y la alta demanda de estos productos en el hogar aumentaron el crecimiento del mercado.
Descargar muestra gratuita para conocer más sobre este informe.
Descripción general del mercado de biopsia líquida y métricas clave
Tamaño del mercado y pronóstico
- Tamaño del mercado en 2025: 11.660 millones de dólares
- Tamaño del mercado en 2026: 14,23 mil millones de dólares
- Tamaño del mercado previsto para 2034: 106.490 millones de dólares
- CAGR: 28,61 % entre 2025 y 2032
Cuota de mercado
- Por región: América del Norte dominó el mercado mundial de biopsias líquidas con una participación del 54,57 % en 2025, impulsada por una mayor adopción de pruebas oncológicas de precisión, innovación de productos y marcos de reembolso favorables en EE. UU. y Canadá.
- Por producto: Los kits y reactivos tuvieron la mayor participación en 2024 debido a los frecuentes lanzamientos de productos y aprobaciones para soluciones de pruebas de ctDNA y NIPT. Empresas como Illumina, Guardant Health y Foundation Medicine están ampliando sus carteras de ensayos para ofrecer pruebas de alta sensibilidad con tiempos de respuesta más rápidos.
Aspectos destacados clave del país
- Estados Unidos: Estados Unidos lidera debido a una fuerte inversión en I+D, ensayos aprobados por la FDA para diagnósticos avanzados de cáncer y la adopción generalizada de pruebas oncológicas caseras posteriores a la COVID-19. Por ejemplo, Guardant360 CDx de Guardant Health fue la primera biopsia líquida aprobada por la FDA para NSCLC.
- India: La creciente incidencia del cáncer (de 1,39 millones en 2020 a 1,46 millones en 2022) ha provocado una mayor demanda de detección temprana del cáncer y NIPT. Las iniciativas de salud nacionales y los datos del ICMR han impulsado la adopción, especialmente en los centros urbanos.
- China: El crecimiento del mercado se ve impulsado por el aumento de la inversión en pruebas genéticas y el creciente envejecimiento de la población. La rápida expansión de los laboratorios de diagnóstico molecular y la innovación local están mejorando el acceso a las pruebas de biopsia líquida tanto para oncología como para detección prenatal.
- Europa: Impulsado por programas gubernamentales de detección del cáncer y aprobaciones regulatorias. El Servicio Nacional de Salud del Reino Unido lanzó programas de detección temprana del cáncer basados en biopsias líquidas, y Alemania y Francia están ampliando la disponibilidad de NIPT. Dxcover Ltd. y otras empresas están recibiendo financiación gubernamental para desarrollar nuevas plataformas.
- Japón: La demanda es alta debido al envejecimiento de la población y al apoyo gubernamental a la detección temprana de trastornos genéticos y cánceres. Los hospitales japoneses están adoptando tecnologías de biopsia líquida basadas en NGS para aplicaciones prenatales y oncológicas.
Tendencias del mercado de biopsia líquida
Aumento del despliegue de productos para el diagnóstico oncológico
La biopsia de tejido para la detección del cáncer se asocia con limitaciones inherentes, como el alto tiempo de respuesta de las pruebas, el gran consumo de tiempo y su naturaleza invasiva. La biopsia líquida está surgiendo como un enfoque novedoso y no invasivo para detectar y monitorear el cáncer en varios fluidos corporales en lugar de en tejido tumoral. Estas pruebas representan una alternativa para los pacientes que no pueden someterse a una biopsia invasiva para la detección, que además ofrece otras aplicaciones clínicas a los pacientes, incluido el pronóstico de la enfermedad, la resistencia a los medicamentos y la respuesta a los medicamentos.
- Según datos publicados por Pharmaceutical Technology en mayo de 2021, aproximadamente entre el 27,0 % y el 31,0 % de los pacientes con carcinoma de pulmón de células no pequeñas (NSCLC) no pueden proporcionar una muestra de tejido adecuada tras el diagnóstico.
Por lo tanto, la demanda del producto es alta debido a varias ventajas sobre los métodos tradicionales. Estos incluyen resultados tempranos, alta sensibilidad y amplia presencia en entornos de atención médica con el potencial de ofrecer información sobre múltiples sitios metastásicos, entre otros.
- En diciembre de 2022, Haymarket Media, Inc. publicó un estudio de cohorte de 170 pacientes recién diagnosticados con cáncer de pulmón de células no pequeñas (NSCLC) en estadio IV. Los resultados indicaron que las muestras de biopsia líquida proporcionaron material suficiente parasecuenciación de próxima generación (NGS), lo que resulta en una tasa de éxito del 100,0%. Sin embargo, las muestras de biopsia de tejido tuvieron una tasa de éxito del 89,2%.
Así, debido a la gran demanda, los fabricantes se centran en desarrollar pruebas de detección temprana de enfermedades con tecnologías avanzadas y amplias aplicaciones. Además, el aumento de las aprobaciones de productos por parte de las autoridades reguladoras para la detección del cáncer, junto con un alto conocimiento de las biopsias líquidas entre los pacientes, ayudan al crecimiento del mercado.
Descargar muestra gratuita para conocer más sobre este informe.
Factores de crecimiento del mercado de biopsia líquida
Aumento de las inversiones en ensayos clínicos por parte de los actores de la industria para impulsar el crecimiento del mercado
Los avances recientes en biopsias líquidas están permitiendo el uso de nuevas tecnologías en la detección del cáncer, la selección terapéutica, la optimización de ensayos de fármacos y el seguimiento de la recurrencia. Varias empresas importantes se están centrando en invertir en I+D para realizar estudios clínicos sobre biopsia líquida para ofrecer medicina de precisión a los pacientes. Esto se debe a la creciente prevalencia del cáncer y a la alta adopción de biopsias líquidas entre los pacientes.
- Por ejemplo, en julio de 2022, Delfi Diagnostics, Inc. recaudó una financiación de 225,0 millones de dólares para el desarrollo de pruebas de biopsia líquida que se utilizarán para la detección del cáncer.
Además, las fuertes inversiones realizadas por organizaciones gubernamentales de todo el mundo para realizar estudios de pruebas clínicas para satisfacer la creciente demanda de este tipo de pruebas en el mercado también están impulsando el crecimiento del mercado. Además, los institutos de investigación ahora están proporcionando fondos a las empresas manufactureras para apoyar la investigación y el desarrollo para la detección temprana y la detección de diversos trastornos genéticos e infecciosos.
- En noviembre de 2021, BioMark Diagnostics Inc., una subsidiaria de BioMark Diagnostic Solutions Inc., recibió una financiación de hasta 135.640,0 dólares del Programa de Asistencia a la Investigación Industrial del Consejo Nacional de Investigación de Canadá (NRC IRAP). La financiación tenía como objetivo apoyar la I+D de su ensayo de biopsia líquida para el cribado y la detección temprana del cáncer de pulmón en pacientes.
Además, la creciente atención de los actores clave de la industria en la colaboración con otras empresas e instituciones de investigación para ofrecer opciones de tratamiento basadas en evidencia con biopsias líquidas para pacientes aumentó aún más el crecimiento del mercado.
- En diciembre de 2022, Guardant Health, Inc. se asoció con Susan G. Komen para realizar estudios clínicos para identificar pacientes con cáncer de mama en etapa temprana con la ayuda de Guardant Reveal, una prueba de sangre.
- En diciembre de 2022, Menarini Silicon Biosystems, Inc., en colaboración con el instituto oncológico Dana-Farber, realizó un estudio clínico que mostró potencial para el tratamiento mínimamente invasivo de pacientes con mieloma múltiple en las primeras etapas de la enfermedad utilizando el sistema CELLSEARCH.
Por lo tanto, se prevé que inversiones tan elevadas por parte de los actores de la industria y una amplia gama de aplicaciones potenciales impulsen la introducción de productos avanzados en los países desarrollados, impulsando aún más el crecimiento del mercado.
FACTORES RESTRICTIVOS
Los altos costos de las pruebas y sus desafíos de reembolso para limitar la adopción del producto
La biopsia líquida está surgiendo como un enfoque complementario a la biopsia de tejido para la detección y el tratamiento de diversas indicaciones, como el cáncer, las pruebas prenatales y otras. Sin embargo, a pesar de las posibles ventajas sobre los enfoques tradicionales en la detección temprana y el seguimiento de enfermedades, el costo asociado con la detección y los kits de prueba es comparativamente alto.
- Por ejemplo, según los datos publicados por Healio en diciembre de 2023, el costo de una biopsia líquida para la detección del cáncer colorrectal es comparativamente más alto que el de una colonoscopia. Para mejorar la adopción entre la población general, el costo de la biopsia líquida tendría que disminuir en un 66,0%.
- Según varios artículos publicados y catálogos de productos de la empresa, una sola prueba de biopsia líquida a menudo puede costar más de 2000 USD en los EE. UU. Según estimaciones del NCBI de julio de 2022, el costo de una prueba Guardant360-NGS puede llegar a los 3557,6 USD en comparación con la recolección de una biopsia de tejido tumoral de 1402,4 USD.
Además, los ensayos basados en la reacción en cadena de la polimerasa (PCR) o la secuenciación de próxima generación (NGS) proporcionan una mejor utilidad clínica y se utilizan ampliamente. Sin embargo, los costos asociados con el desarrollo de esas tecnologías son muy altos. Estos factores, junto con los altos costos de inversión en la realización de diversos estudios clínicos para la detección, están frenando el crecimiento del mercado.
Además, el uso de estas pruebas para la detección temprana se ve limitado por problemas de reembolso causados por la precisión de las pruebas y los resultados clínicos inciertos. La falta de cobertura de seguro para resultados clínicos específicos, como el seguimiento de recaídas, la recurrencia, los cánceres en estadios III y IV avanzados y otros, limita la adopción de estas pruebas para la detección. Esto resultó en menos incentivos para que las empresas desarrollaran pruebas para la detección del cáncer.
- Según datos publicados por el NCBI en 2021, se afirmó que los Centros de Servicios de Medicare y Medicaid (CMS) no brindan cobertura de seguro para pruebas de biopsia líquida para detección y restringen la cobertura a afecciones que incluyen metástasis, recurrencia o cánceres avanzados en estadio III y IV.
Además, la falta de conciencia y la falta de disponibilidad de cobertura de seguro en países en desarrollo como India, China y Sudáfrica para tales pruebas restringe aún más el crecimiento del mercado en estos países.
Los factores mencionados anteriormente y la falta de utilidad clínica de estas pruebas están limitando su adopción. Se prevé que esto obstaculice el crecimiento del mercado durante el período de pronóstico.
Análisis de segmentación del mercado de biopsia líquida
Por análisis de producto
Aumento del lanzamiento de kits de ensayos tecnológicamente avanzados para aumentar la participación en el segmento
Por producto, el mercado se segmenta en kits, reactivos e instrumentos. Se espera que el segmento de kits y reactivos represente el 80,08% del mercado en 2026. El dominio se atribuyó al creciente enfoque de los actores clave para expandir su huella y reforzar su presencia en el mercado a través del lanzamiento de nuevos productos. Además, muchos actores de la industria están introduciendo versiones avanzadas de sus kits de ensayos de diagnóstico existentes para proporcionar resultados más rápidos y confiables.
- Por ejemplo, en noviembre de 2023, Illumina Inc. lanzó una segunda versión del kit TruSight Oncology 500 ctDNA para permitir el perfil genómico de tumores sólidos. Esta segunda versión del kit de ensayo proporciona resultados más rápidos con mayor sensibilidad, lo que permite una medicina de precisión.
- En febrero de 2021, Guardant Health, Inc. lanzó una prueba de revelación Guardant para la monitorización de enfermedades residuales y recurrencia en pacientes con cáncer colorrectal en etapa temprana. La prueba detecta la enfermedad residual después de la cirugía y la recurrencia meses antes que los métodos de atención estándar actuales.
Además, el aumento en la aprobación de ensayos y kits y el aumento de las políticas de reembolso comercial por parte de las autoridades reguladoras en las economías desarrolladas impulsaron aún más el crecimiento del segmento.
- Según los datos publicados por el Instituto Nacional del Cáncer (NCI), en noviembre de 2021, la FDA amplió la aprobación de la prueba FoundationOne Liquid CDx en la detección y terapia del cáncer de ovario y de mama. La FDA aprobó la prueba a principios de 2020 para identificar pacientes con cáncer de pulmón y próstata que reciben medicamentos dirigidos específicos.
Por otro lado, se espera que el segmento de instrumentos registre una CAGR moderada durante el período de pronóstico. El crecimiento del segmento se atribuye al aumento de las inversiones en producción y lanzamiento de nuevos instrumentos y equipos por parte de actores clave.
- En septiembre de 2021, Thermo Fisher Scientific lanzó el sistema de PCR digital QuantStudio Absolute Q de Applied Biosystems. El sistema utiliza tecnología de matriz de microfluidos y flujos de trabajo simplificados para ejecutar ensayos de biopsia líquida para identificar mutaciones genéticas y cancerosas.
Para saber cómo nuestro informe puede ayudar a optimizar su negocio, Hable con un analista
Por análisis de aplicaciones
Preferencia creciente de pruebas prenatales no invasivas entre mujeres embarazadas para aumentar el crecimiento del segmento
Según la aplicación, el mercado se clasifica enPruebas prenatales no invasivas (NIPT), oncología y otros.
Se prevé que el segmento de pruebas prenatales no invasivas (NIPT) tenga una cuota de mercado dominante del 68,69% en 2026.Esta proporción se atribuyó al aumento de anomalías genéticas y congénitas, como el síndrome de Down, en el feto de mujeres embarazadas en todo el mundo. De manera similar, la gran demanda de pruebas de detección no invasivas entre las mujeres y el aumento de las aprobaciones de productos de pruebas prenatales avanzadas lanzadas por actores clave impulsaron aún más la participación segmentaria.
- Según un artículo publicado por el grupo de las Naciones Unidas en marzo de 2022, la incidencia estimada del síndrome de Down se sitúa entre 1 de cada 1.000 y 1 de cada 1.100 nacidos vivos en todo el mundo. Además, cada año nacen aproximadamente entre 3.000 y 5.000 niños con este trastorno cromosómico.
- En mayo de 2021, Yourgene anunció el lanzamiento de IONA care, una oferta de servicios de pruebas prenatales no invasivas (NIPT). La solución proporcionó un beneficio ampliado al medir la probabilidad de que una mujer embarazada tenga un feto con aneuploidías de los cromosomas sexuales (SCA1) y aneuploidías autosómicas (AA2), junto con la detección de trisomías 21, 18 y 13 y la determinación del sexo del feto.
Se proyecta que el segmento de oncología registre una CAGR comparativamente más alta durante el período de pronóstico. Esto se debe al creciente interés de los actores de la industria por ofrecer pruebas avanzadas para satisfacer la creciente demanda de diagnóstico temprano y seguimiento de diversas enfermedades no transmisibles como el cáncer. Además, las crecientes asociaciones entre actores clave para comercializar su cartera de productos e impulsar su presencia global impulsaron aún más la participación en el segmento.
- En junio de 2021, Guardant Health, Inc. amplió su cartera de productos añadiendo Guardant360 Response, una prueba de sangre para inmunoterapia y terapia dirigida.
Por análisis del usuario final
Aumento de la demanda de pruebas en entornos hospitalariospara impulsar el crecimiento del segmento
Según el usuario final, el mercado se divide en hospitales, laboratorios clínicos y otros.
Se espera que el segmento de hospitales represente el 75,01% del mercado en 2026. La participación dominante se puede atribuir al creciente número de pruebas de diagnóstico de cáncer y pruebas prenatales en hospitales de todo el mundo. Otro factor que favorece el crecimiento del segmento es la creciente concienciación sobre la detección del cáncer entre la población, especialmente en los países emergentes.
- Según un artículo publicado en el Informe Anual de Revisión de Genómica y Genética Humana en agosto de 2021, aproximadamente entre el 25,0% y el 30,0% de las mujeres embarazadas en Australia se someten a NIPT en hospitales privados.
Se espera que el segmento de laboratorios clínicos crezca a una tasa compuesta anual considerable durante el período de pronóstico. El crecimiento del segmento se debe al creciente número de laboratorios clínicos que proporcionan biopsias líquidas en los países en desarrollo.
- Según un artículo publicado por Laboratory of Florida LLC., en 2021, más de 200.000 laboratorios clínicos brindaron servicios de pruebas en los EE. UU. Según estimaciones adicionales, alrededor de 5.414 laboratorios independientes realizaron el 32,0% del total de pruebas en los EE. UU.
PERSPECTIVAS REGIONALES
Aumento de la introducción de productos tecnológicamente avanzados para aumentar la cuota de mercado de América del Norte
Según la región, el mercado está segmentado en América del Norte, Asia Pacífico, Europa, América Latina y Oriente Medio y África.
North America Liquid Biopsy Market Size, 2025 (USD Billion)
Para obtener más información sobre el análisis regional de este mercado, Descargar muestra gratuita
América del norte
El mercado de América del Norte generó 6.360 millones de dólares en 2025, lo que representa el 54,57% del panorama del mercado mundial, y se espera que alcance los 7.750 millones de dólares en 2026. La expansión del mercado está impulsada por el aumento de la I+D y la introducción de nuevas tecnologías por parte de actores clave para ayudar en la detección de trastornos o anomalías crónicas en los pacientes. Además, varias empresas de ciencias biológicas están proporcionando soluciones de prueba de biopsia líquida en varias regiones para brindar terapias dirigidas a pacientes con cáncer. Además, las crecientes colaboraciones entre los actores del sector manufacturero y las crecientes aprobaciones de nuevos productos con una amplia presencia regional mejoraron aún más el mercado de América del Norte. Se prevé que el mercado estadounidense alcance los 7.330 millones de dólares en 2026.
- Por ejemplo, en mayo de 2023, Labcorp lanzó una nueva prueba de biopsia líquida para pacientes con tumores sólidos metastásicos. Esta prueba evalúa el ADN circulante liberado por las células tumorales y ayuda a los oncólogos a gestionar la atención del paciente mediante planes de terapia dirigida.
- En noviembre de 2022, Thermo Fisher Scientific presentó ensayos de biopsia líquida por PCR digital para su sistema dPCR Q absoluto de Applied Biosystems y una herramienta de diseño personalizado para simplificar la investigación del cáncer en institutos de investigación clínica y académica.
Europa
Europa contribuyó con el 24,50% del mercado global en 2025, con una valoración de 2.860 millones de dólares, y se prevé que alcance los 3.480 millones de dólares en 2026. Europa es la segunda región dominante en términos de cuota de mercado e ingresos. El mercado europeo tuvo una participación significativa debido a la creciente concienciación sobre el cáncer y los exámenes prenatales entre la población. Además, varios actores del mercado se están centrando en recibir financiación para el desarrollo de una plataforma de biopsia líquida con la ayuda de tecnologías avanzadas. De manera similar, el aumento de las iniciativas estratégicas del gobierno europeo para impulsar la detección del cáncer junto con otras pruebas de patología fortalecerá aún más el crecimiento regional durante el período previsto. Se espera que el mercado del Reino Unido alcance los 460 millones de dólares en 2026, mientras que el mercado de Alemania alcance los 1010 millones de dólares en 2026.
- Por ejemplo, en febrero de 2023, Dxcover Limited recaudó casi 12,4 millones de dólares (10 millones de libras esterlinas) para el desarrollo de una nueva plataforma de biopsia líquida para la detección de diferentes tipos de cáncer.
- En marzo de 2022, se informó que el Servicio Nacional de Salud del Reino Unido ofrecía pruebas de biopsia líquida a ciertos pacientes con cáncer como complemento a las pruebas de patología anatómica con un esfuerzo por diagnosticar el 75,0% de todos los cánceres en etapa I o etapa II para el año 2028.
- Según los datos publicados por el MDPI en 2022, alrededor de 6.560 pacientes se benefician anualmente de pruebas de biopsia líquida para el cribado del cáncer de pulmón de células no pequeñas (CPCNP) en Europa.
Asia Pacífico
Asia Pacífico representó 2.130 millones de dólares en 2025, lo que representa el 18,22% de la cuota de mercado mundial, y se prevé que alcance los 2.620 millones de dólares en 2026. La creciente prevalencia de anomalías genéticas, como el síndrome de Down y las aneuploidías cromosómicas, entre la población impulsa el crecimiento del mercado en Asia Pacífico. Se anticipa que la región exhibirá la CAGR más alta durante el período de estudio. Esto se debe a la creciente demanda de exámenes predictivos debido a la alta prevalencia de enfermedades. Se prevé que el mercado de Japón alcance los 720 millones de dólares en 2026, el mercado de China alcance los 550 millones de dólares en 2026 y el mercado de la India alcance los 390 millones de dólares en 2026.
- Según un artículo de ScienceDirect publicado en diciembre de 2022, un estudio afirmó que entre 2016 y 2020, se informaron aproximadamente 265 biopsias líquidas anuales con síndrome de Down (1 de cada 1158) en Australia.
América Latina
América Latina contribuyó aproximadamente con 220 millones de dólares al mercado mundial en 2025, lo que representa una participación del 1,90 %, y se espera que alcance los 270 millones de dólares en 2026. Se prevé que el mercado de América Latina crezca a un ritmo más lento durante el período previsto. El crecimiento se debe a la creciente prevalencia del cáncer entre la población y a la gran demanda de pruebas de detección del cáncer en hospitales y laboratorios de patología.
Medio Oriente y África
En 2025, Oriente Medio y África poseían el 0,80% del mercado mundial, alcanzando una valoración de 0,09 mil millones de dólares, y se prevé que crezca a 110 millones de dólares en 2026. Se espera que Oriente Medio y África crezcan a una tasa compuesta anual moderada debido al aumento de las pruebas NIPT entre las mujeres embarazadas, lo que creará una demanda de biopsias líquidas no invasivas durante el período previsto.
Lista de empresas clave en el mercado de biopsia líquida
Colaboraciones estratégicas entre actores clave para ofrecer oportunidades de crecimiento para el mercado
La industria está dominada principalmente por fabricantes como Guardant Health, Inc., Foundation Medicine, Personalis, Inc. y otros actores destacados. Los actores clave apuntan a acelerar la producción de pruebas y recibir aprobaciones de productos de varios organismos reguladores, lo que es responsable de su mayor participación en el mercado de biopsias líquidas.
- En mayo de 2021, Guardant Health, Inc. recibió la aprobación de la FDA de EE. UU. para la prueba Guardant360 CDx como la primera y única prueba para el diagnóstico de cáncer de pulmón de células no pequeñas avanzado.
Otros actores importantes que operan en el mercado, como F. Hoffmann-La Roche Ltd, se están centrando en desarrollos clave, como asociaciones estratégicas con otras instituciones de investigación de todo el mundo, para desarrollar pruebas de detección y seguimiento eficaces para los pacientes. Se espera que este tipo de iniciativas por parte de actores importantes impulsen el mercado global durante el período de pronóstico.
- En junio de 2022, F. Hoffmann-La Roche Ltd. se asoció con la Lung Cancer Research Foundation (LCRF) y el Lung Cancer Mutation Consortium (LCMC) para participar en LCMC 4.thensayo de detección para evaluar factores accionables en el cáncer de pulmón en etapa temprana para ofrecer opciones de terapia dirigida a los pacientes.
Además, otros actores que operan en el mercado global incluyen Menarini Silicon Biosystems, Inc., Thermo Fisher Scientific Inc., QIAGEN, Bio-Rad Laboratories, Inc., BioChain Institute Inc., Stilla, BIOCEPT, INC. y GRAIL, LLC. El sólido enfoque en la realización de diversos estudios clínicos para ofrecer ensayos de alta precisión para el diagnóstico de enfermedades y la selección de terapias es responsable de la alta tasa de crecimiento del mercado de otros actores.
Este compromiso continuo en el lanzamiento de pruebas de diagnóstico por parte de varios actores del mercado y un creciente enfoque en colaboraciones con otras organizaciones para establecer sus huellas en las pruebas de detección impulsarán aún más la expansión del mercado.
LISTA DE EMPRESAS CLAVE PERFILADAS:
- Salud guardián(A NOSOTROS.)
- PERSONALIS, INC.(A NOSOTROS.)
- FUNDACIÓN MEDICINA, INC. (EE.UU.)
- Natera, Inc. (Estados Unidos)
- Illumina, Inc. (EE. UU.)
- F. Hoffmann-La Roche Ltd (Suiza)
- Menarini Silicon Biosystems, Inc. (Italia)
- Thermo Fisher Scientific Inc. (EE. UU.)
- QIAGEN(Alemania)
- Bio-Rad Laboratories, Inc. (EE. UU.)
DESARROLLOS CLAVE DE LA INDUSTRIA:
- Febrero de 2024:Twist Bioscience Corporation presentó un kit de preparación de bibliotecas de cfDNA para respaldar la investigación de biopsias líquidas.
- Mayo de 2022:Guardant Health, Inc. anunció que los servicios de pruebas de cáncer basados en muestras de sangre en Europa están operativos en las instalaciones de pruebas de biopsia líquida del Instituto Vall d'Hebron de Oncología (VHIO) en Barcelona.
- abril 2022:Stilla Technologies se asoció con Promega Corporation para ofrecer una solución completa de flujo de trabajo de PCR digital para una amplia gama de aplicaciones para la investigación del cáncer. Estos incluyeron biopsia líquida, pruebas de patógenos centinela y otros.
- septiembre 2021:Thermo Fisher Scientific Inc. colaboró con AstraZeneca para desarrollar NGS (CDx) para respaldar la cartera en expansión de terapias dirigidas de AstraZeneca.
- Julio de 2021:QIAGEN colaboró con Sysmex Corporation para desarrollar cáncerdiagnóstico complementarioutilizando tecnología de secuenciador de próxima generación de biopsia líquida ultrasensible.
- Junio de 2021:Illumina Inc. y Next Generation Genomic Co., Ltd. lanzaron la solución VeriSeq NIPT v2 en el sudeste asiático.
COBERTURA DEL INFORME
El informe proporciona un análisis de mercado detallado y se centra en aspectos cruciales como los principales actores, los tipos de productos y las principales aplicaciones del producto. Además, ofrece información sobre las tendencias del mercado y desarrollos clave de la industria, como fusiones, asociaciones y adquisiciones. Además de los factores mencionados anteriormente, el informe incluye los factores que han contribuido al crecimiento del mercado en los últimos años con un análisis regional de diferentes segmentos.
Solicitud de personalización para obtener un conocimiento amplio del mercado.
Alcance y segmentación del informe
|
ATRIBUTO |
DETALLES |
|
Período de estudio |
2021-2034 |
|
Año base |
2025 |
|
Año estimado |
2026 |
|
Período de pronóstico |
2026-2034 |
|
Período histórico |
2021-2024 |
|
Índice de crecimiento |
CAGR del 28,61% entre 2026 y 2034 |
|
Unidad |
Valor (millones de dólares) |
|
Segmentación |
Por producto
|
|
Por aplicación
|
|
|
Por usuario final
|
|
|
Por región
|
Preguntas frecuentes
Fortune Business Insights dice que se prevé que el mercado global crezca de 14,23 mil millones de dólares en 2026 a 106,49 mil millones de dólares en 2034.
Con una tasa compuesta anual del 28,61%, el mercado exhibirá un crecimiento constante durante el período previsto (2026-2034).
Por producto, se espera que el segmento de kits y reactivos lidere este mercado durante el período de pronóstico.
La creciente prevalencia del cáncer y la creciente I+D de productos tecnológicamente avanzados en todo el mundo son los factores clave que impulsan el crecimiento del mercado.
Guardant Health, Inc., Foundation Medicine y Natera, Inc. son los principales actores del mercado global. Guardant Health, Inc., Foundation Medicine y Natera, Inc. son los principales actores del mercado global.
Se espera que la creciente prevalencia de trastornos genéticos en los fetos de mujeres embarazadas y un aumento en el número de pruebas de detección del cáncer en todo el mundo impulsen la adopción de estas pruebas.
Póngase en contacto con nuestras expertas Habla con un experto
Obtenga un 20% de personalización gratuita
Ampliar la cobertura regional y por país, Análisis de segmentos, Perfiles de empresas, Benchmarking competitivo, e información sobre el usuario final.
Informes relacionados
- Mercado de diagnóstico complementario
- Mercado de servicios de pruebas genéticas
- Mercado de biomarcadores
- Mercado de detección del cáncer de hígado
- Mercado de detección del cáncer de pulmón
- Mercado de diagnóstico molecular de oncología
- Mercado de detección de cáncer colorrectal
- Mercado de pruebas prenatales no invasivas