바이오프로세스 검증 시장 규모, 점유율 및 산업 분석, 테스트 유형별(추출물 및 침출물 테스트, 미생물학적 테스트, 호환성 테스트, 무결성 테스트, 물리화학적 테스트 등), 모드별(사내 및 아웃소싱), 검증 영역별(프로세스 검증, 세척 검증, 분석 방법 검증, 장비 검증 및 기타), 의약품별(단클론 항체, 재조합 단백질, 백신, 세포 및 유전자 치료법, 바이오시밀러 등), 최종 사용자별(제약 및 생명공학 회사 등) 및 지역 예측(2026~2034년)
바이오프로세스 검증 시장 개요
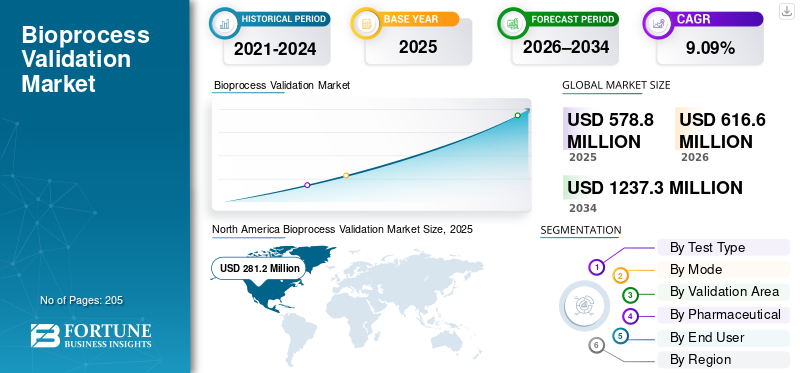
2025년 전 세계 바이오프로세스 검증 시장 규모는 5억 7,880만 달러로 평가되었습니다. 시장은 2026년 6억 1,660만 달러에서 2034년까지 12억 3,730만 달러로 성장하여 예측 기간 동안 CAGR 9.09%를 나타낼 것으로 예상됩니다.북미는 2025년에 48.58%의 시장 점유율로 바이오프로세스 검증 시장을 지배했습니다.
바이오프로세스 검증은 바이오의약품 제조 프로세스가 안전하고 효과적인 생물학적 제제를 일관되게 생산하도록 보장합니다. 단일클론항체 생산, 백신 생산, 세포/세포 생산 등 바이오제조 공정이 진행되고 있음을 입증하는 문서화된 증거입니다.유전자 치료또는 재조합 단백질은 의도한 상업적 규모에서 사전 정의된 제품 품질 특성 및 규제 요구 사항을 충족하는 제품을 지속적으로 생산합니다. 이 시장은 혁신적인 생물학적 제제 개발에 대한 관심이 높아짐에 따라 크게 성장하고 있습니다.
시장의 주요 업체로는 Merck KGaA, Eurofins Scientific, SGS Société Générale de Surveillance SA, Sartorius AG 등이 있습니다. 이들 회사는 서비스 제공의 기술 발전에 중점을 두고 있습니다.
무료 샘플 다운로드 이 보고서에 대해 더 알아보려면.
생물공정 밸리데이션 시장 동향
CDMO에 대한 아웃소싱은 눈에 띄는 시장 추세입니다.
최근 몇 년 동안 시장은 자체 검증에서 아웃소싱 검증 서비스로 전환하고 있습니다. 바이오프로세스 검증 작업은 더욱 전문화되고 있으며 기업은 내부 QA/검증 팀을 영구적으로 확장하기보다는 더 빠른 일정과 가변적인 용량을 추구합니다. 바이오 제조 발자국이 세계화됨에 따라 기업은 현장 전반에 걸쳐 일관된 GMP 문서, 표준화된 실행 및 감사 준비 데이터를 보장하기 위해 아웃소싱도 합니다. 이러한 경향은 기술 이전, 용량 확장, 문제 해결 프로젝트, 내부 팀이 대역폭 제약에 직면할 때 특히 강합니다. 또한 아웃소싱은 고정 비용 부담을 줄이고 내부 유지 관리 비용이 많이 드는 틈새 전문 지식과 고급 장비에 대한 액세스를 제공합니다. 이러한 요인들은 전반적인 글로벌 바이오프로세스 검증 시장 성장을 지원하고 있습니다.
- 예를 들어, 2024년 10월 SGS는 미국 링컨셔 현장에서 바이오의약품 테스트 역량 확장을 발표했으며, 이 시설이 현재 제약, 바이오의약품 및 제약 분야의 개발자와 제조업체에 아웃소싱 서비스를 제공하고 있음을 명시적으로 밝혔습니다.의료기기
무료 샘플 다운로드 이 보고서에 대해 더 알아보려면.
시장 역학
시장 동인
증가하는 글로벌 생물의약품 및 바이오시밀러 파이프라인 검증 수요 증가로 시장 성장 촉진
시장은 주로 생물학적 제제의 급속한 확장에 의해 주도되고 있습니다.바이오시밀러관로. 이는 각각의 새로운 분자가 개발에서 상업적 규모로 이동하여 새로운 공정 검증(PPQ/CPV), 분석 방법 검증/이전, 세척 검증 및 GMP 준비에 대한 광범위한 문서화를 촉발하기 때문입니다. 스폰서가 더 많은 바이오시밀러 자산을 추가함에 따라 사이트/CDMO 전반에 걸쳐 비교 작업, 변경 제어 및 기술 이전도 증가하며, 각 단계에서는 일관성과 제어를 입증하기 위한 검증 지원이 필요합니다. 또한 운영 회사 간의 협력 증가도 시장 확장을 지원합니다.
- 예를 들어, 2024년 7월 Evotec은 바이오시밀러 개발 및 상업적 제조를 위해 Sandoz와의 전략적 파트너십을 확대했습니다.
시장 제약
시장 성장을 방해하는 높은 분석 복잡성과 전문 기술 전문성의 필요성
높은 분석 복잡성은 생물학적 제제, 백신 및 CGT 제품이 광범위한 민감한 분석 패널을 필요로 하는 경우가 많으며 각 방법을 검증하고 전송하며 현장 전체에서 통제된 상태로 유지해야 하기 때문에 시장의 제약이 됩니다. 이로 인해 검증 프로젝트의 비용과 시간이 증가하고 실행이 부족한 전문가에 의존하게 됩니다. 깊이 있는 전문 지식이 부족하고 방법의 견고성 문제와 문서화 격차로 인해 편차가 발생하고, 연구를 반복하고, 배치 출시 또는 기술 이전 일정이 지연되어 프로그램 확대가 직접적으로 느려질 수 있습니다. 동일한 복잡성으로 인해 고급 계측 및 정교한 데이터 처리에 대한 의존도가 높아져 소규모 업체가 사내에서 유지 관리하는 데 어려움을 겪을 수 있습니다. 결과적으로 프로젝트는 전문가 역량에 병목 현상이 발생하여 서비스 가격이 부풀려지고 리드 타임이 연장될 수 있습니다. 이로 인해 시장 성장이 어느 정도 제한됩니다.
- 예를 들어, 2025년 3월 미국 FDA는 부적절한 분석 방법 검증 관행을 포함한 결함에 대해 Aspen Biopharma Labs Private Limited에 경고 서한을 발행했으며, 이러한 실패가 약물 품질 결함의 위험을 증가시킨다는 점을 지적했습니다.
시장 기회
시장 확장을 위한 수익성 있는 기회를 제공하기 위한 일회용 기술 채택
일회용 기술(SUT)의 채택은 검증 서비스 제공업체에게 강력한 시장 기회입니다. 모든 새로운 일회용 흐름 경로는 GMP 기대치를 충족하기 위해 E&L(추출물 및 침출물), 무결성 및 호환성 증거에 대한 필요성을 증가시킵니다. 제조업체가 SUT 사용을 PD에서 상업용 제품군으로 확장함에 따라 일회성 연구가 아닌 반복 가능하고 표준화된 검증 패키지가 점점 더 필요해지고 있습니다. 이러한 기회는 잦은 전환과 공급업체 변경으로 인해 반복적인 검증 작업 부하가 발생하는 CDMO 주도의 다중 제품 시설에서 특히 매력적입니다. 전반적으로 SUT 웨이브는 고객이 감사 준비가 된 문서 및 해석을 추구함에 따라 실험실 테스트를 넘어 서비스로서의 검증을 위한 주소 지정 가능한 기반을 확장합니다. 예를 들어, 2024년 4월 Cytiva는 대규모 mAb를 위한 Xcellerex 소형 일회용 자기 혼합 시스템을 공개했습니다.백신, 첨단치료제 제조.
시장의 과제
전문 테스트 실험실의 공급망 및 용량 제약시장 성장에 대한 눈에 띄는 도전 제기
공급망 중단과 제한된 전문 테스트 역량은 지속적인 시장 과제입니다. 검증 일정은 부족한 실험실 공간, 소모품/시약의 긴 리드 타임, 숙련된 분석가의 가용성에 따라 달라지는 경우가 많습니다. 실험실에서 갑작스러운 수요 급증에 직면하면 백로그로 인해 처리 시간이 연장되어 배치 릴리스, PPQ 일정 및 패키지 제출이 지연됩니다. 또한, 공급망 변동성으로 인해 실험실에서는 대체 시약/재료를 검증해야 하므로 재작업이 추가되고 처리량이 느려집니다. 이는 테스트를 기다리면 배송이 차단될 수 있는 고가의 생물학적 제제 및 유통기한이 짧은 양식의 경우 특히 고통스럽습니다. 결과적으로 바이오 제조업체는 점점 더 다중 실험실 비상 계획을 필요로 하고 프리미엄/신속 서비스를 지향하게 되어 비용과 계획 복잡성이 증가합니다. 모든 요소가 시장 성장에 누적적으로 영향을 미칩니다.
세분화 분석
테스트 유형별
추출물 및 침출물 테스트 부문 성장을 촉진하기 위한 SUT 채택 증가로 인한 수요 증가
테스트 유형에 따라 시장은 추출물 및 침출물 테스트, 미생물 테스트, 호환성 테스트, 무결성 테스트, 물리화학적 테스트 등으로 구분됩니다.
추출물 및 여과물 테스트 부문은 세계 최대의 바이오프로세스 검증 시장 점유율을 차지했습니다. 바이오 제조는 일회용 시스템으로 크게 전환되었으며, 모든 폴리머 접촉 표면은 특성화되고 문서화되어야 하는 직접적인 환자 안전 및 규정 준수 위험을 야기합니다. SUS 채택이 프로세스 개발에서 상업 생산으로 확장됨에 따라 기업에는 일반적으로 일상적인 물리화학 또는 호환성 검사보다 더 전문적이고 가치가 높은 반복 가능한 E&L 패키지가 필요합니다. 이로 인해 운영업체들은 규제 승인을 받아 서비스 제공을 확장하는 데 주력하고 있습니다.
- 예를 들어, 2025년 5월 SGS는 추출 가능 물질 및 침출 가능 물질 테스트를 제공하기 위해 캐나다 제약 실험실에 대해 ISO 17025 인증을 받았다고 발표했습니다.
무결성 테스트 부문은 예측 기간 동안 CAGR 10.56%로 증가할 것으로 예상됩니다.
이 보고서가 비즈니스 최적화에 어떻게 도움이 되는지 알아보려면, 애널리스트와 상담
모드별
사내 부문 성장을 촉진하기 위해 내부 제조에 대한 높은 투자
모드에 따라 시장은 사내 및 아웃소싱으로 구분됩니다.
2025년에는 사내 부문이 글로벌 시장을 장악했습니다.바이오의약품제조업체는 품질 시스템 내에 핵심 검증 활동을 포함시키는 것을 선호합니다. 이는 일관된 SOP, 보다 빠른 내부 승인, GMP 문서 및 배치 영향 결정에 대한 보다 엄격한 제어를 보장함으로써 규제 위험을 줄입니다. 사내 팀은 또한 사소한 변경이 CQA에 영향을 미칠 수 있는 생물학제제에 특히 중요한 프로세스 노하우/IP를 보호합니다. 이것이 바로 새로운 생물학적 제제 시설에 투자하는 기업이 본질적으로 대규모 내부 검증 조직을 필요로 하는 강력한 내부 실험실/제조 인프라를 구축하는 경우가 많은 이유입니다. 또한 이 부문은 2026년에 59.6%의 점유율을 차지할 것으로 예상됩니다.
- 예를 들어, 2025년 4월 머크는 델라웨어 주 윌밍턴에 출시 및 상업 생산을 지원하기 위한 실험실 및 제조 역량으로 구성된 10억 달러 규모의 생물의약품 우수 센터를 설립했다고 발표했습니다.
아웃소싱 부문은 예측 기간 동안 CAGR 10.61%로 증가할 것으로 예상됩니다.
검증 영역별
장비 자격 부문 성장을 촉진하기 위한 검증에서의 높은 활용도
검증 영역을 기준으로 시장은 프로세스 검증, 세척 검증, 분석 방법 검증, 장비 검증 등으로 구분됩니다.
장비 검증 부문은 2025년 세계 시장에서 가장 높은 점유율을 차지했습니다. 이는 GMP 자산을 장비 및 유틸리티로 가져오기 위한 필수 단계이며, 프로세스 작업이 확장되기 전에 전체 클린룸 시스템이 올바르게 설치되고 일관되게 작동하는지 입증해야 하는 경우가 많습니다. 프로세스 또는 청소 검증과 달리 검증은 모든 신규 구축, 용량 확장, 장비 교체, 자동화 업그레이드 및 주요 변경 제어에 의해 트리거되므로 현장 수명주기 전반에 걸쳐 반복적으로 발생합니다. 또한 노동 집약적이며 여러 분야를 다루므로 서비스 지출이 늘어납니다. 또한 이 부문은 2026년에 27.5%의 점유율을 차지할 것으로 예상됩니다.
- 예를 들어, 2025년 11월 Exyte는 타당성부터 적격 인도까지 GMP 시설의 엔드투엔드 제공을 지원하기 위해 Pharmaplan 통합을 완료했습니다.
분석 방법 검증 부문은 예측 기간 동안 CAGR 10.62%로 증가할 것으로 예상됩니다.
제약별
단일클론항체의 파이프라인 확장으로 분절적 우세를 뒷받침
의약품을 기준으로 시장은 단일클론 항체, 재조합 단백질, 백신,세포 및 유전자 치료법, 바이오시밀러 등이 있습니다.
단일클론항체 부문은 2025년에 가장 큰 시장 점유율을 차지할 것으로 예상됩니다. 이는 여러 가지 시판 제품과 강력한 임상 파이프라인을 갖춘 상업용 생물의약품 제조의 가장 큰 설치 기반입니다. 또한, mAb는 점점 더 mAb 포트폴리오 및 관련 플랫폼과 같은 더 높은 가치의 양식에 포함되어 새로운 시설, 장비 적격성 평가 주기, 적격성/검증 패키지를 추진하고 있습니다. 또한 이 부문은 2026년에 36.5%의 점유율을 차지할 것으로 예상됩니다.
- 예를 들어, 2025년 9월 Eli Lilly는 버지니아에 50억 달러 규모의 제조 시설을 건설할 계획을 발표했습니다. 이 시설은 Lilly의 새로운 바이오접합 플랫폼과 단일클론 항체 포트폴리오를 위한 전용 부지로 설명됩니다.
세포 및 유전자 치료 부문은 예측 기간 동안 연평균 성장률(CAGR) 16.27%로 상승할 것으로 예상됩니다.
최종 사용자별
강력한 생물학적 제제 확장 및 GMP 투자로 제약 및 생명공학 기업 부문 성장 지원
최종 사용자를 기준으로 시장은 다음과 같이 분류됩니다.제약및 생명 공학 회사, 계약 개발 및 제조 조직 등.
2025년에는 제약 및 생명공학 기업 부문이 글로벌 시장에서 선두 자리를 차지했습니다. 이들 회사는 생물학제 포트폴리오 개발에 적극적으로 참여하고 있으며 GMP 제조 네트워크의 최대 운영업체입니다. 또한, 바이오제약 회사의 투자 증가는 부문 성장을 지원합니다. 또한 2026년에는 68.2%의 점유율을 차지할 것으로 예상된다.
- 예를 들어, 2025년 9월 Gilead Sciences는 생물학적 제제 역량과 역량을 강화하기 위해 새로운 미국 제조 허브를 출범시켰습니다.
또한 계약 개발 및 제조 조직 부문은 예측 기간 동안 CAGR 12.01%로 성장할 것으로 예상됩니다.
바이오프로세스 검증 시장 지역 전망
지역별로 시장은 북미, 유럽, 아시아 태평양, 라틴 아메리카, 중동 및 아프리카로 분류됩니다.
북아메리카
North America Bioprocess Validation Market Size, 2025 (USD Million)
이 시장의 지역 분석에 대한 추가 정보를 얻으려면, 무료 샘플 다운로드
2024년 북미 시장 규모는 2억 6,880만 달러로 글로벌 시장을 장악했다. 이 지역은 또한 2025년에도 2억 8,120만 달러로 선두를 유지했습니다. 지역적 지배력은 빠르게 확장되는 생물제제 및 바이오시밀러 파이프라인, 강력한 규제 지원, 지역 내 고급 CDMO의 존재에 의해 주도됩니다.
미국 바이오프로세스 검증 시장
미국 시장은 북미 시장의 주요 점유율을 차지했으며 분석적으로 추정하면 2026년 약 2억 7,380만 달러로 글로벌 시장의 약 44.4%를 차지합니다.
아시아 태평양
아시아 태평양 시장 규모는 2026년에 1억 5,010만 달러로 평가될 것으로 예상됩니다. 해당 지역은 업계에서 두 번째로 큰 지역의 위치를 확보할 것으로 예상됩니다. 특히 중국, 인도에서의 생물제제 제조의 급속한 확장, CDMO 투자 증가 등의 요인이 지역 시장 성장의 원인이 됩니다.
일본 바이오프로세스 검증 시장
2026년 일본 시장은 약 2,210만 달러로 추정되며, 이는 전 세계 매출의 약 3.6%를 차지합니다.
중국 바이오프로세스 검증 시장
중국 시장은 2026년에 약 4,300만 달러의 매출을 달성할 것으로 예상되며, 이는 전 세계 매출의 약 7.0%를 차지합니다.
인도 바이오프로세스 검증 시장
2026년 인도 시장은 약 2,620만 달러로 전 세계 매출의 약 4.3%를 차지할 것으로 추산됩니다.
유럽
유럽 시장은 예측 기간 동안 CAGR 7.70%로 성장할 것으로 예상됩니다. 이 지역은 전체 지역 중에서 세 번째로 높은 지역이 될 것으로 예상됩니다. 지역 시장은 주로 강력한 생명공학 클러스터의 존재, 지원적인 EMA 규정, 유럽 국가 전반의 CDMO 생태계 확장에 의해 주도됩니다.
영국 바이오프로세스 검증 시장
2026년 영국 시장은 약 2,480만 달러로 추정되며, 이는 전 세계 매출의 약 4.0%를 차지합니다.
독일 바이오프로세스 검증 시장
독일 시장 규모는 2026년 약 2,920만 달러에 이를 것으로 예상되며, 이는 전 세계 매출의 약 4.7%에 해당합니다.
라틴 아메리카, 중동 및 아프리카
라틴 아메리카, 중동 및 아프리카 지역은 연구 기간 동안 상대적으로 느리게 성장할 것입니다. 라틴 아메리카 시장 규모는 2026년에 2,840만 달러의 가치에 도달할 것으로 예상됩니다. 이러한 지역 성장은 주로 신흥 바이오 제조와 이 지역의 선택적 아웃소싱 증가에 의해 주도됩니다.
중동 및 아프리카 지역 중 2026년 GCC 시장은 약 950만 달러로 추정되며, 이는 전 세계 매출의 약 1.5%를 차지합니다.
경쟁 환경
주요 산업 플레이어
전문화된 테스트 용량 및 디지털 검증 서비스의 전략적 확장으로 경쟁 포지셔닝이 재편되고 있습니다.
글로벌 바이오프로세스 검증 시장은 다소 세분화되어 있습니다. 주요 플레이어로는 Eurofins Scientific, SGS, Nelson Labs(Sotera Health), Charles River Laboratories, Thermo Fisher Scientific Inc., MerckKGaA 및 Sartorius가 있습니다. 이들 기업은 용량 확장, 추출물 및 침출물 역량 강화, 무균성 보증, 미생물학 발자국 확장을 위한 M&A, 디지털/AI 기반 검증 워크플로우를 가속화하기 위한 파트너십에 중점을 두고 있습니다.
- 예를 들어, 2025년 6월 Nelson Labs는 무균 보증 서비스에 대한 수요 증가와 엄격한 EU GMP Annex 1 요구 사항을 충족하기 위해 솔트레이크시티 본사의 ISO 등급 클린룸 용량을 두 배로 늘리는 확장 프로젝트를 발표했습니다.
시장의 다른 주요 업체로는 Laboratory Corporation of America Holdings, DOC S.r.l., Hangzhou Cobetter Filtration Equipments Co., Ltd, Meissner Filtration Products, Inc. 등이 있습니다. 이들 회사는 다양한 애플리케이션에 걸쳐 혁신적인 서비스를 적극적으로 제공하고 있습니다.
프로파일링된 주요 생물공정 검증 회사 목록
- 머크 KGaA(독일)
- 유로핀스 사이언티픽 (룩셈부르크)
- SGS Société Générale de Surveillance SA(스위스)
- 사토리우스 AG(독일)
- 시티바(다나허)(우리를.)
- Laboratory Corporation of America Holdings(미국)
- DOC S.r.l. (이탈리아)
- Hangzhou Cobetter Filtration Equipments Co., Ltd (중국)
- Meissner Filtration Products, Inc.(미국)
- 찰스 리버 연구소. (우리를.)
주요 산업 발전
- 2025년 12월:Sikich는 ValGenesis의 AI 기반 디지털 검증 플랫폼을 생명 과학 고객에게 제공하고 검증 프로세스를 현대화하기 위해 ValGenesis와의 전략적 파트너십을 발표했습니다.
- 2025년 10월:Intertek Pharmaceutical Services는 새로운 한국 약전 요구 사항 준수를 지원하기 위해 E&L(추출물 및 침출물) 테스트 서비스를 시작했습니다.
- 2025년 10월:Alcami는 생물학제제/CGT(방법 확립, 방출/안정성 및 특성화)에 대한 분석 역량을 강화하기 위해 노스캐롤라이나주 더럼에서 20,000평방피트 규모의 실험실 서비스 확장을 발표했습니다.
- 2025년 7월:ValGenesis는 검증 수명 주기 관리(디지털 검증)의 글로벌 확장과 AI 기반 혁신을 가속화하기 위해 최대 1,600만 달러의 전략적 자금 조달을 발표했습니다.
- 2024년 9월:Pace Life Sciences는 노스캐롤라이나주 RTP에 있는 Catalent의 분석 서비스 연구소를 인수하여 검증 프로그램을 지원하는 분석 서비스의 용량/역량을 확장한다고 발표했습니다.
보고서 범위
커스터마이징 요청 광범위한 시장 정보를 얻기 위해.
보고서 범위 및 세분화
| 기인하다 | 세부 |
| 학습기간 | 2021년부터 2034년까지 |
| 기준 연도 | 2025년 |
| 추정연도 | 2026년 |
| 예측기간 | 2026년부터 2034년까지 |
| 역사적 기간 | 2021-2024 |
| 성장률 | 2026~2034년 CAGR 9.09% |
| 단위 | 가치(백만 달러) |
| 분할 | 테스트 유형, 모드, 검증 영역, 제약, 최종 사용자 및 지역별 |
| 테스트 유형별 |
|
| 모드별 |
|
| 신청별 |
|
| 제약별 |
|
| 최종 사용자 기준 |
|
| 지역별 |
|
자주 묻는 질문
Fortune Business Insights에 따르면 글로벌 시장 가치는 2025년 5억 7,880만 달러였으며, 2034년에는 12억 3,730만 달러에 이를 것으로 예상됩니다.
2025년 북미 시장 가치는 2억 8,120만 달러였습니다.
시장은 예측 기간 동안 9.09%의 CAGR을 보일 것으로 예상됩니다.
테스트 유형별로는 추출물 및 여과물 테스트 부문이 시장을 주도했습니다.
증가하는 글로벌 생물의약품 및 바이오시밀러 파이프라인과 그에 따른 검증 수요 증가가 시장을 이끄는 주요 요인입니다.
Merck KGaA, Eurofins Scientific, SGS Société Générale de Surveillance SA 및 Sartorius AG는 글로벌 시장에서 저명한 기업 중 일부입니다.
2025년에는 북미가 가장 큰 점유율로 시장을 장악했습니다.
전문가에게 문의하세요 전문가와 상담하세요
20% 무료 맞춤 설정 받기
지역 및 국가 범위 확장, 세그먼트 분석, 기업 프로필, 경쟁 벤치마킹, 및 최종 사용자 인사이트.