제약 품질 관리 및 규정 준수 시장 규모, 점유율 및 산업 분석, 제공별(제품{기기 및 소모품}, 소프트웨어 및 서비스), 애플리케이션별(소분자 의약품, 생물학적 제제 및 바이오시밀러, 백신, 세포 및 유전자 치료법 및 기타) 기능별(원료 품질 관리, 미생물학 및 오염 관리, 안정성 및 유효 기간 테스트, 공정 중 품질 관리, 완제품 테스트 및 배치 출시, 기타), 최종 사용자별(제약 및 생명공학 회사, CRO 및 CDMO 등) 및 지역 예측, 2026~2034년
제약 품질 관리 및 규정 준수 시장 규모 및 향후 전망
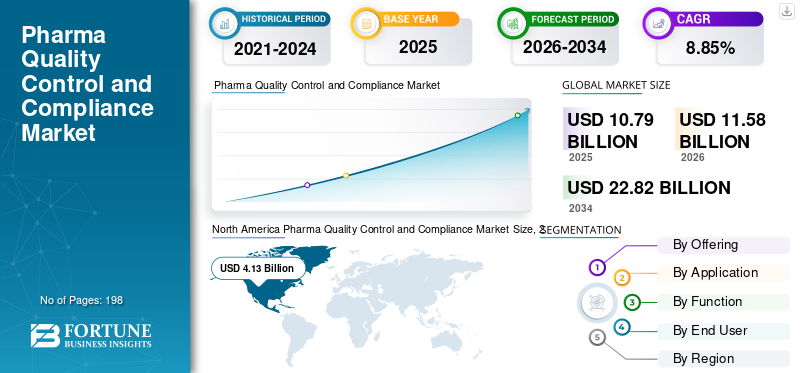
전 세계 제약 품질 관리 및 규정 준수 시장 규모는 2025년 107억 9천만 달러로 평가되었습니다. 시장은 2026년 115억 8천만 달러에서 2034년까지 228억 2천만 달러로 성장하여 예측 기간 동안 CAGR 8.85%를 나타낼 것으로 예상됩니다.
제약 품질 관리 및 규정 준수 시스템은 의약품 품질을 평가하고, GMP 규정 준수를 보장하고, 규제 문서를 감독하고, 원자재, 공정 중 배치, 완제품, 미생물학적 테스트, 안정성 및 검증 프로세스와 관련된 출시 결정을 지원하는 데 활용됩니다. 제약 및 생명공학 회사가 QC 도구, 소모품, 디지털 품질 시스템 및 아웃소싱 GMP 테스트에 대한 투자를 늘려 소분자, 생물학제제, 의약품 등의 제조 복잡성이 증가함에 따라 시장이 확대되고 있습니다.백신, 세포 및 유전자 치료법. 감사 준비 및 규제 준수를 향상시키는 클라우드 기반 품질 관리 시스템과 함께 오염 제어, 데이터 무결성, 배치 릴리스 효율성, 검증 및 적격성 평가 프로세스에 대한 강조가 높아짐에 따라 수요가 더욱 강화됩니다.
글로벌 시장에서 활동하는 주요 업체로는 Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation, Sartorius AG 등이 있습니다. 이들 기업은 시장 입지를 유지하기 위해 제품의 기술 발전, 전략적 협력, 포트폴리오 확장에 주력하고 있습니다.
무료 샘플 다운로드 이 보고서에 대해 더 알아보려면.
제약 품질 관리 및 규정 준수 시장 동향
자동화된 규정 준수 솔루션으로의 전환은 글로벌 시장에서 관찰되는 중요한 추세입니다.
제약 및 생명공학 기업은 수동적이고 종이 기반이며 분리된 품질 프로세스에서 편차, CAPA, 문서 관리, 교육, 배치 검토 및 감사 준비를 보다 일관되게 처리할 수 있는 자동화 시스템으로 전환하고 있습니다. 이러한 변화는 규제 대상 제조업체가 점점 더 복잡해지는 운영 내에서 더 빠른 의사 결정, 향상된 추적성, 감소된 문서 오류 및 향상된 데이터 무결성을 요구함에 따라 발생합니다. 자동화된 규정 준수 도구는 기업이 다양한 위치에서 절차를 표준화하고, 검토 주기 기간을 단축하고, 검사 및 GMP 감사 준비를 강화하는 데 도움을 줍니다. 생물학적 제제, 멸균 제품, 고급 치료법이 증가하면서 이러한 추세는 더욱 강화되고 있으며, 이로 인해 실시간으로 처리해야 하는 품질 이벤트 및 규정 준수 문서의 양이 증가하고 있습니다. 결과적으로 제약 회사는 품질, 제조 및 규제 시스템을 연결하는 eQMS, LIMS, 디지털 배치 릴리스 및 AI 기반 워크플로우 플랫폼에 더 많은 리소스를 투자하고 있습니다.
- 예를 들어, 2025년 1월 Honeywell은 디지털 혁신과 고급 자동화를 통해 생명과학 조직이 통합 제조 및 품질 관리에 접근하는 방식을 변화시키도록 설계된 TrackWise 생명과학 플랫폼을 출시했습니다.
시장 역학
시장 동인
무료 샘플 다운로드 이 보고서에 대해 더 알아보려면.
시장 성장을 촉진하기 위한 약물 개발 활동 증가로 인한 수요 증가
강화된 약물 개발 활동으로 인한 수요 증가는 제약 품질 관리 및 규정 준수 시장 성장을 이끄는 주요 요인입니다. 제약 및 생명공학 회사는 원료, 공정 중 관리, 미생물학, 안정성 연구, 검증 및 배치 출시 지원에 대한 테스트를 강화해야 하는 소분자, 생물학적 제제 및 첨단 치료법을 포함하도록 파이프라인을 확장하고 있습니다. 개발 프로그램의 증가로 인해 후보자가 개발에서 임상 및 상업 제조로 전환함에 따라 GMP 준수 분석 방법, 향상된 문서화 시스템 및 더욱 엄격한 규정 준수 관리에 대한 수요도 높아졌습니다. 이는 QC 장비, 소모품, 고품질 소프트웨어 및 아웃소싱 테스트/규정 준수 서비스에 대한 필요성을 직접적으로 향상시킵니다.
- 예를 들어, 2025년 4월 노바티스는 10개 시설을 포함해 7개 시설을 포함해 미국 기반 제조 및 R&D 입지를 확장하기 위해 5년에 걸쳐 230억 달러를 투자할 계획을 발표했습니다.
시장 제약
시장 성장을 제한하는 엄격한 규제 요건
엄격한 규제 요건은 GMP 준수 운영을 유지하는 데 필요한 비용, 복잡성 및 시간을 증가시키기 때문에 주요 시장 제한 사항입니다. 의약품 제조업체는 FDA, EMA 및 기타 규제 표준을 충족하기 위해 검증된 시스템, 문서 관리, 품질 감독, 데이터 무결성, 환경 모니터링, 직원 교육 및 감사 준비에 많은 투자를 해야 합니다. 품질 단위 감독, 청소 검증, 오염 제어 또는 배치 문서화에 사소한 차이라도 경고 편지, 교정 비용, 제품 출시 지연 또는 공급 중단을 유발할 수 있습니다. 이러한 요구 사항은 특히 소규모 제조업체와 생물학적 제제, 멸균 제품 또는 다중 현장 글로벌 운영으로 확장하는 기업에 부담이 됩니다. 엄격한 규정은 제품 안전을 지원하지만 운영 비용을 높이고 새로운 프로세스, 시설 및 제품 이전의 구현을 느리게 만듭니다.
- 예를 들어, 2025년 8월 미국 FDA는 2025년 3월 인도 구자라트에 있는 시설을 검사한 후 Amneal Pharmaceuticals에 경고 서한을 발행했습니다. 이 서한에는 완제품 의약품에 대한 심각한 CGMP 위반 사항이 요약되어 있으며, 규정 위반으로 인해 어떻게 규제 조치, 개선 부담, 잠재적인 운영 중단이 발생할 수 있는지 설명되어 있습니다.
시장 기회
시장 성장 기회 제공을 위한 아웃소싱 품질 관리 서비스 채택 증가
아웃소싱 품질 관리 서비스의 사용 증가는 제약 품질 관리 및 규정 준수 부문에 중요한 기회를 제공합니다. 제약 및 생명공학 기업은 상당한 내부 자본 지출 없이 더 빠른 처리 시간, GMP 인증 실험실 역량, 향상된 분석 기술을 달성하기 위해 점차적으로 QC 업무를 전문 파트너에게 위임하고 있습니다. 이는 생물학적 제제, 백신, 세포 및유전자 치료법점점 더 복잡해지는 출하 테스트, 오염 관리, 분석법 검증 및 안정성 지원이 필요해졌습니다. 아웃소싱은 기업이 변동하는 생산량을 처리하고 내부 QA/QC 팀의 스트레스를 완화하며 확장 또는 다중 사이트 생산 중 유연성을 향상시키는 데 도움이 됩니다. 또한, 국제 서비스 제공업체는 다양한 지역에서 표준화된 테스트를 촉진할 수 있으며, 이는 여러 규제 시장에서 활동하는 기업에 도움이 됩니다.
- 예를 들어 Eurofins Scientific 및 Charles River Laboratories는 품질 관리 서비스를 제공하는 회사 중 일부입니다.
시장의 과제
글로벌 공급망 전반에 걸쳐 일관된 품질 표준을 유지하는 복잡성시장 성장에 대한 눈에 띄는 도전 제시
글로벌 공급망 전반에 걸쳐 균일한 품질 표준을 보장하는 과제는 의약품 품질 관리 및 규정 준수 시장에서 중요한 문제입니다. 제약회사는 API, 부형제, 중간체,포장재, 다양한 국가의 완제품 제조 지원으로 인해 모든 현장과 공급업체에서 일관된 GMP 실행을 유지하는 것이 복잡해졌습니다. 공급업체 품질 시스템, 문서화 방법론, 테스트 강도, 데이터 무결성 측정 및 규제 개발의 변화로 인해 규정 준수 위험이 증가하는 불일치가 발생할 수 있습니다. 이 문제는 기업이 생물학적 제제, 멸균 의약품 또는 대량의 제네릭에 대한 광범위한 다층 공급망을 처리할 때 점점 더 중요해지며, 사소한 품질 결함이라도 배치 출시를 연기하거나 교정을 시작할 수 있습니다. 또한 다양한 지역에 걸쳐 공급업체 자격, 감사 프로그램, 오염 제어, 추적성 및 통합 품질 관리 시스템의 필요성이 높아집니다. 결과적으로 기업은 글로벌 운영이 조화롭게 유지되도록 감독, 검증, 디지털 품질 솔루션 및 제3자 테스트에 더 많은 투자를 해야 합니다.
- 예를 들어, 2025년 7월 WHO는 오염된 의약품이 의약품 부형제의 글로벌 공급망의 전신적 취약성으로 인해 발생하는 경우가 많다는 점을 지적했습니다.
세분화 분석
제공으로
QC 장비 및 소모품의 광범위한 사용으로 제품 부문이 지배하게 되었습니다.
제공 측면에서 시장은 제품, 소프트웨어 및 서비스로 구분됩니다. 제품 부문은 기기와 소모품으로 더 구분됩니다.
제품 부문은 2025년 글로벌 제약 품질 관리 및 규정 준수 시장 점유율을 주도했습니다. 이 부문의 지배력은 일상 생활에서 기기 및 소모품의 중요한 기능에 기인합니다.제약 품질 관리원자재 분석, 공정 중 평가, 미생물학적 평가, 무균성 평가, 안정성 테스트 및 완제품의 배치 출시를 포함한 작업을 수행합니다. 또한 규제 대상인 각 제조 시설에는 실질적인 QC 조치가 필요하므로 크로마토그래피 시스템, 미생물 테스트 장비, 모니터링 기기, 시약, 배지, 필터 및 참조 물질에 대한 비용이 지속적으로 증가합니다.
- 예를 들어, 2024년 5월 Sartorius는 멸균 테스트를 위한 4세대 Sterisart Universal 펌프 출시를 발표했습니다. 이 시스템은 제약 및 생명공학 산업의 엄격한 품질 및 안전 표준을 충족하는 동시에 더 강력한 데이터 무결성 및 감사 준비를 위해 21 CFR Part 11 준수 문서를 지원하도록 설계되었습니다.
소프트웨어 부문은 예측 기간 동안 CAGR 12.03%로 성장할 것으로 예상됩니다.
이 보고서가 비즈니스 최적화에 어떻게 도움이 되는지 알아보려면, 애널리스트와 상담
애플리케이션별
소분자 약물의 광범위한 제조 기반이 부문별 지배력을 뒷받침함
응용 분야에 따라 시장은 저분자 의약품, 생물학적 제제 및 의약품으로 분류됩니다.바이오시밀러, 백신, 세포 및 유전자 치료법 등.
저분자 의약품 부문은 정제, 캡슐, 주사제 및 기타 전통적인 의약품에 대한 광범위한 전 세계 제조 능력으로 인해 지배적인 점유율을 차지했으며, 이로 인해 원료 테스트, 공정 중 검사, 용출 평가, 불순물 평가, 안정성 연구 및 완제품의 배치 출시에 대한 중요하고 지속적인 수요가 발생했습니다. 또한 저분자 제품은 고급 방식보다 더 많은 위치에서 더 큰 배치 볼륨으로 제조되므로 QC 장비, 소모품 및 규정 준수 시스템에 대한 지출이 안정적으로 유지됩니다. 또한 이 부문은 2026년에 54.3%의 점유율을 차지할 것으로 예상됩니다.
- 예를 들어, 2025년 10월 머크는 버지니아 주 엘크턴에 30억 달러 규모의 제약 우수 센터 착공을 시작했습니다. 회사는 확장에 활성 제약 성분과 소분자 제조 및 테스트를 지원하는 의약품 투자가 모두 포함된다고 밝혔습니다.
백신 부문은 예측 기간 동안 CAGR 9.22%로 상승할 것으로 예상됩니다.
기능별
상업적 출시 전 최종 품질 검증의 필요성으로 인해 해당 부문이 지배하게 되었습니다.
기능을 기준으로 시장은 원료 품질 관리, 미생물학 및 오염 관리, 안정성 및 유효 기간 테스트, 공정 중 품질 관리, 완제품 테스트 및 배치 출시, 규정 준수 관리, 검증 및 적격성 평가/품질 시스템 관리 등으로 구분됩니다.
2025년 시장은 완제품 테스트 및 배치 출시 부문이 주로 주도했으며 2026년에는 21.3%의 점유율을 차지할 예정입니다. 이 부문의 지배력은 각 의약품 배치가 선적 전에 최종 사양 확인을 거쳐야 하는 필요성에서 비롯되며 이 기능은 저분자 및 생물학적 생산 모두에 필수적입니다. 또한 완제품 테스트에는 분석, 불순물, 용해, 무균성, 효능 및 문서 검토 활동이 결합되어 있으므로 QC 및 규정 준수 비용의 상당 부분을 차지합니다. 배치 릴리스 단계의 지연은 제품 가용성, 운전 자본 및 시장 출시 시간에 직접적인 영향을 미칠 수 있으므로 제조업체는 더 빠르고 안정적이며 더 잘 연결된 릴리스 프로세스에 계속 투자하고 있습니다. 최종 제품 검증 및 출시 준비에 대한 지속적인 요구 사항은 해당 부문의 강력한 시장 위치를 강화합니다.
- 예를 들어, 2025년 5월 Veeva는 중앙 집중화되고 자동화된 접근 방식을 통해 복잡한 배치 릴리스 워크플로를 간소화하고 제품 공급 결정을 개선해야 할 필요성이 커지고 있음을 강조했습니다.
규정 준수 관리 부문은 예측 기간 동안 CAGR 10.84%로 성장할 것으로 예상됩니다.
최종 사용자별
제약 및 생명공학 회사는 품질 관리 및 규정 준수에 대한 높은 지출로 인해 수요를 주도했습니다.
최종 사용자를 기준으로 시장은 다음과 같이 분류됩니다.제약및 생명 공학 회사, CRO 및 CDMO 등.
제약 및 생명공학 기업 부문은 약물 개발, 제조, 배치 출시 및 규제 준수 책임을 직접 소유하면서 2025년 시장을 지배했습니다. 또한 내부 제조 네트워크 전반에 걸쳐 GMP 표준을 유지하는 데 필요한 QC 기기, 소모품, 품질 소프트웨어, 미생물학 시스템, 검증 도구 및 규정 준수 서비스의 주요 구매자입니다. 원자재 테스트부터 완제품 출시까지 제품 품질을 관리하기 때문에 전반적인 가치 측면에서 지출은 아웃소싱 업체보다 여전히 높습니다. 또한 이 부문은 2026년에 71.4%의 점유율을 차지할 것으로 예상됩니다.
- 예를 들어, 2024년 7월 Biogen은 노스캐롤라이나에 20억 달러 규모의 제조 투자를 발표했습니다. 회사는 자사 캠퍼스에 의약품의 안전성, 효능 및 순도를 보장하기 위한 정교한 품질 관리 실험실이 포함되어 있다고 밝혔습니다.
또한 CRO/CDMO는 예측 기간 동안 10.95%의 성장률을 보일 것으로 예상됩니다.
제약 품질 관리 및 규정 준수 시장 지역 전망
지리에 따라 시장은 라틴 아메리카, 아시아 태평양, 유럽, 북미, 중동 및 아프리카로 구분됩니다.
북아메리카
North America Pharma Quality Control and Compliance Market Size, 2025 (USD Billion)
이 시장의 지역 분석에 대한 추가 정보를 얻으려면, 무료 샘플 다운로드
북미는 2024년 38억 8천만 달러로 시장 점유율 1위를 차지했고, 2025년에도 41억 3천만 달러로 선두를 유지했다. 북미는 제약, 생명공학, 첨단치료제 생산 분야의 탄탄한 기반을 바탕으로 확장되고 있습니다. 이 지역에서는 GMP 준수, 검증, 멸균 보증, 배치 출시 테스트 및 디지털 품질 시스템을 위해 상당한 자금을 할당합니다.
미국 제약 품질 관리 및 규정 준수 시장
미국 시장은 북미를 주도하며 2026년에는 약 38억 5천만 달러 규모로 글로벌 시장의 약 33.3%를 차지할 것으로 예상된다.
유럽
유럽 시장은 광범위한 의약품 제조 네트워크, 강력한 생물학적 제제 및 백신 생산 기반, 잘 확립된 GMP 환경에 힘입어 예측 기간 동안 CAGR 7.90%로 성장할 것으로 예상됩니다. 이 지역은 또한 아웃소싱 QC 테스트 및 규정 준수 서비스를 지원하는 강력한 CDMO 존재의 이점을 누리고 있습니다.
영국 제약 품질 관리 및 규정 준수 시장
영국 시장은 2026년 약 4억 8천만 달러로 추정되며, 이는 전 세계 매출의 약 4.2%를 차지합니다.
독일 제약 품질 관리 및 규정 준수 시장
독일은 2026년에 약 6억 7천만 달러에 달할 것으로 예상되며 이는 전 세계 매출의 약 5.8%에 해당합니다.
아시아 태평양
아시아 태평양 지역의 시장 규모는 2026년에 27억 6천만 달러에 달할 것으로 예상되며, 중국과 인도의 의약품 생산 능력이 빠르게 증가함에 따라 가장 빠르게 성장하는 지역입니다. 이 지역에서는 현지 공급 및 수출 시장을 활성화하기 위해 QC 실험실, 미생물학 테스트, 오염 관리 및 GMP 준수 제조 시스템에 대한 투자가 증가하고 있습니다.
일본 제약 품질 관리 및 규정 준수 시장
2026년에 일본은 5억 6천만 달러에 도달하여 전 세계 매출의 약 4.9%를 차지할 것으로 예상됩니다.
중국 제약 품질 관리 및 규정 준수 시장
중국 시장은 2026년 약 8억 9천만 달러에 달할 것으로 예상되며, 이는 전 세계 매출의 약 7.7%를 차지합니다.
인도 제약 품질 관리 및 규정 준수 시장
2026년 인도는 5억 2천만 달러에 달해 전 세계 매출의 약 4.5%를 차지할 것으로 예상됩니다.
라틴 아메리카, 중동 및 아프리카
라틴 아메리카, 중동 및 아프리카의 성장은 현지 의약품 제조에 대한 투자 증가, 규제 준수에 대한 관심 증가, 수입 의약품에 대한 의존도 감소 노력에 힘입어 향후 몇 년간 온건할 것으로 예상됩니다. 2026년 이 지역 시장 규모는 약 7억 5천만 달러로 추산됩니다.
GCC 시장은 2026년에 약 2억 달러에 달할 것으로 예상되며, 이는 전 세계 매출의 약 1.8%를 차지합니다.
경쟁 환경
주요 산업 플레이어
통합 QC 포트폴리오 및 디지털 규정 준수 기능 확장으로 플레이어 시장 위치 지원
글로벌 시장은 Thermo Fisher Scientific Inc., Agilent Technologies Inc., Waters Corporation, Sartorius AG 및 상당한 수익을 창출하는 기타 주요 기업으로 구성된 반분절화된 경쟁 환경을 반영합니다. 이들 회사의 상당한 시장 입지는 광범위한 포트폴리오와 강력한 지리적 입지로 뒷받침됩니다. 또한 이들 플레이어는 QA, QC, 교육, 검증, 배치 릴리스 및 규정 준수 워크플로를 연결하는 통합 품질 생태계에 중점을 두고 있으며, 이는 경쟁 우위를 강화할 것으로 예상됩니다.
다른 중요한 참가자로는 Charles River Laboratories, Eurofins Scientific, LabVantage Solutions Inc. 및 LabWare가 있습니다. 이들 기업은 시장 지위를 높이기 위해 제품 개선, 통합 제품, 신제품 출시에 주력할 것으로 예상됩니다.
- 예를 들어 2024년 8월 Veeva Systems는 Veeva Vault Quality와 통합된 클라우드 기반 QC 솔루션인 Veeva Vault LIMS의 모멘텀이 커지고 있다고 발표했습니다. 회사는 이 설정이 생명 과학 회사가 QA와 QC 프로세스를 연결하고, 종이 기반 문서를 줄이고, 더 많은 정보를 바탕으로 배치 출시 결정을 지원하는 데 도움이 된다고 밝혔습니다.
주요 제약 품질 관리 및 규정 준수 회사 목록
- 써모 피셔 사이언티픽(주)(우리를.)
- 애질런트 테크놀로지스, Inc.(우리를.)
- 워터스 코퍼레이션(우리를.)
- Veeva 시스템(우리를.)
- 하니웰 인터내셔널(미국)
- Sartorius AG (독일)
- 찰스 리버 연구소(미국)
- Eurofins Scientific(룩셈부르크)
- LabVantage Solutions Inc.(미국)
- 랩웨어(미국)
주요 산업 발전
- 2026년 1월:Charles River는 PathoQuest를 인수하겠다는 의사를 밝혔습니다. Charles River는 이번 계약을 통해 외래성 인자를 식별하고 세포주 및 바이러스 벡터의 특성을 파악하기 위한 PathoQuest의 iDTECT 품질 관리 플랫폼과 같은 신속하고 진보된 GMP 테스트 솔루션을 통합함으로써 자사의 생물학적 제제 테스트 능력을 향상시킬 것이라고 밝혔습니다.
- 2025년 5월:Waters Corporation은 Empower 소프트웨어가 이제 Wyatt MALS 및 RI 장비의 생물학 데이터 수집 및 QC 분석을 지원한다고 발표했습니다.
- 2025년 3월:LabVantage는 LIMS 플랫폼의 최신 버전인 LabVantage 8.9를 출시했습니다. 이 업데이트는 규제된 QC 환경과 관련된 자동화 및 AI 기반 효율성을 추가하여 실험실 생산성을 향상시키고 정확성과 규정 준수를 보장하며 복잡한 작업 흐름을 단순화하도록 설계되었습니다.
- 2025년 3월:LabWare는 LabWare QAQC 및 LabWare GROW와 함께 LabWare ASSURE를 통해 SaaS 포트폴리오를 확장했습니다.
- 2025년 1월:Veeva와 Zifo는 품질 관리 현대화를 가속화하기 위한 공동 제품 노력을 공개했습니다. 통합을 통해 Veeva LIMS를 Zifo의 qcKen 플랫폼과 병합하면 기업이 소스 문서 또는 다른 LIMS 시스템에서 데이터를 가져올 수 있어 마스터 데이터 설정 문제가 완화되고 LIMS 구현 및 사이트 배포가 가속화됩니다.
보고서 범위
글로벌 제약 품질 관리 및 규정 준수 시장 분석에는 보고서에서 강조된 모든 부문에 대한 시장 규모 및 예측에 대한 철저한 평가가 포함됩니다. 이는 예측 기간 동안 시장을 주도할 것으로 예상되는 시장 역학 및 추세에 대한 통찰력을 제공합니다. 기술 진보, 제품 혁신, 규제 환경, 신제품 출시 등 필수 요소에 대한 이해를 제공합니다. 또한 파트너십, 인수 합병은 물론 시장 내 업계의 주요 개발에 대해 자세히 설명합니다. 이 보고서는 또한 시장 점유율에 대한 정보와 주요 활성 플레이어의 프로필을 포함하여 심층적인 경쟁 환경을 제공합니다.
커스터마이징 요청 광범위한 시장 정보를 얻기 위해.
보고서 범위 및 세분화
| 기인하다 | 세부 |
| 학습기간 | 2021년부터 2034년까지 |
| 기준 연도 | 2025년 |
| 추정연도 | 2026년 |
| 예측기간 | 2026년부터 2034년까지 |
| 역사적 기간 | 2021-2024 |
| 성장률 | 2026~2034년 CAGR 8.85% |
| 단위 | 가치(미화 10억 달러) |
| 분할 | 오퍼링, 애플리케이션, 기능, 최종 사용자 및 지역별 |
| 제공으로 |
|
| 애플리케이션별 |
|
| 기능별 |
|
| 최종 사용자별 |
|
| 지역별 |
|
자주 묻는 질문
Fortune Business Insights에 따르면 글로벌 시장 가치는 2025년 107억 9천만 달러였으며 2034년에는 228억 2천만 달러에 이를 것으로 예상됩니다.
2025년 북미 시장 가치는 41억 3천만 달러에 이르렀습니다.
시장은 2026~2034년 예측 기간 동안 8.85%의 CAGR을 보일 것으로 예상됩니다.
제공함으로써 제품 부문이 시장을 선도할 것으로 예상됩니다.
약물 개발 활동 증가, 오염 제어에 대한 집중 강화, CRO/CDMO에 대한 아웃소싱 증가로 인한 수요 증가가 주로 시장 확장을 주도하고 있습니다.
Thermo Fisher Scientific Inc., Agilent Technologies, Waters Corporation 및 Sartorius AG는 글로벌 시장에서 저명한 기업 중 일부입니다.
2025년에는 북미가 시장을 장악했습니다.
전문가에게 문의하세요 전문가와 상담하세요
20% 무료 맞춤 설정 받기
지역 및 국가 범위 확장, 세그먼트 분석, 기업 프로필, 경쟁 벤치마킹, 및 최종 사용자 인사이트.